Indoor Living Soil - Die Grundlagen
Honorary mentions und Einführung in die Living Soil Community
Ich versuche hiermit möglichst gut mein bisher gesammeltes Wissen zum Thema Living Soil zusammenzutragen. Es wird versucht, mit den aktuellen wissenschaftlichen Erkenntnissen zu arbeiten, welche jedoch ständig im Wandel sind. Daher können manche der hier dargelegten Informationen schon wieder widerlegt sein. Viele Techniken sind auch noch nicht explizit für Cannabis erforscht worden und zu mehrzyklischen Bodensystemen auf Torfbasis gibt es auch nicht viel Forschung. Deshalb versuche ich hier fundiert anekdotische und wissenschaftliche Erkenntnisse zu kombinieren, um euch einen möglichst umfangreichen und effektiven Guide zum Gärtnern mit Living soil für Cannabis an die Hand zu geben.
Ich freue mich bereits auf angeregte Diskussionen und auch von euch zu lernen. Ich bitte nur um einen wissenschaftlichen Argumentationsstil, d.h. so weit es geht mit Quellen zu arbeiten und wenn es keine gibt, mit Daten und eigenen Erfahrungen zu argumentieren.
Erreichen kann man mich über die Instagram Accounts @Bavarian_buds oder @Research-gardens oder über die Kommentarfunktion
Dieser Artikel basiert auf meinem Studium der Gartenbauwissenschaften, den Studien zum Bodenfruchtbarkeitsprinzip nach William Albrecht, dem Podcast „Cannabis Science and Cultivation“ von Tad Hussey, der Beratung durch Bryant Mason zu meinen Bodenproben/Werten und vielen Leuten aus den Foren wie z.B. Jonathan Traxler oder Ninos Farm aus der Indoor Living soil Community, deren Rezepte und Tipps als Basis für den Beispielbodenmix verwendet werden, welcher im dritten Teil der Artikelreihe enthalten ist.
Der Plan für diese Artikelreihe ist es, in drei Teilen die nötigen Grundlagen zum eigenständigen Zusammenstellen und Anbau eines „Living Soil“ Systems zu geben.
Dieser erste Teil wird sich um das generelle Konzept, Nachhaltigkeitsaspekte und die Grundlagen eines „guten“ Bodens für Cannabis drehen. Es werden die drei Dimensionen, in denen guter Boden bewertet wird (Physikalisch/Chemisch/Biologisch), aufgeschlüsselt und die wichtigsten Einflussfaktoren aufgezeigt. Dieser erste Teil kann smit als Grundwissen-Artikel zu Living Soil angesehen werden.
Der zweite Teil wird sich um die Übersetzung der vorher aufgelisteten Qualitätsmerkmale in die Bodenzusammenstellung der Basisstoffe, wie z.B. Torf, Minerale und Komposte drehen. Es folgt sowohl eine Erklärung der Testmethoden und Qualitätsmerkmale der einzelnen Stoffe als auch des zusammengemischten Bodens, um daraus In-Prozess-Kontrollwerte zu ermitteln, um die Produktion möglichst zu standardisieren und zu optimieren.
Im dritten und letzten Teil dieser Artikel-Serie gehen wir auf die Kulturführung des Bodens ein, denn diese ist mindestens genauso erfolgsentscheidend wie die richtige Zusammenstellung des Mixes. Zum Schluss werde ich noch eine Aufstellung und einen Excel Rechner meines präferierten Mixes anfügen für die Leser, die direkt mit einem durchdachten Mix starten möchten.
Das Konzept Living Soil und der Begriff Modified Growing Mix
Definition
Indoor living soil erfährt zurzeit einen regelrechten Hype in der Cannabis-Szene, der auch mit der Verbreitung einiger Falschinformationen einher geht, welche Bereinigung erfordern. Ein richtiger Living Soil, so wie er ursprünglich in der Permakulturbewegung bei Cannabis bezeichnet wurde, beschreibt einen Outdoorboden in einem spezifischen Mikroklima mit lokalen Einflüssen von Wind, Wetter und nativem Boden, welcher den Pflanzenbedürfnissen angepasst mit organischen und mineralischen Nährstoffen wie bspw. Kompost oder Gesteinsmehlen, angereichert wird. Living soil schließt idealerweise ein komplettes Ökosystem ein, welches wir nur leicht beeinflussen können, welches aber, bei richtigen Voraussetzungen, sehr stark positiv auf die Kultivierung einwirken kann. So kann eine optimale Balance des Systems z.B. durch vermehrte Vogelnistangebote auch starken Schädlingsdruck aushalten.
Über Zeit entsteht hier ein eigenes Biotop und bei richtiger Pflege stellt sich ein Gleichgewicht ein - Dies regelt die meisten Probleme von selbst wie z.B. Nährstoffmängel oder drastischen Schädlingsbefall. Diese Balance müssen wir im Indoorsystem aus dem Nichts schaffen und können nur teilweise auf etablierte Biotope wie sie draußen zu finden sind, zurückgreifen.
Des Weiteren arbeiten wir hier mit nativem Boden aus den Gefügen Sand, Schluff, Ton und Gestein. Dies ist indoor schwer umsetzbar bzw. wurde damit noch nicht viel experimentiert. Meine bisher erhaltenen anekdotischen Hinweise, warum ein torfbasiertes System besser funktioniert, beschränken sich auf die hohe Aggregationsstabilität des Torfs über Zeit, ein gutes Porenverhältnis, eine hohe Kationenaustauschkapazität und den niedrigen PH des Torf, der eine hohe Anreicherung von Kationen wie Calcium/Magnesium ermöglicht. Daraus folgt, dass wir für den „indoor living soil“ eigentlich gar keinen „Soil“ verwenden, sondern einen „soilless“ Mix, wie man ihn im englischsprachigen Bereich bezeichnet. Durch die Zugabe von Gesteinsmehlen und anderen Nährstoffquellen modifizieren wir diesen „soilless“ Mix noch weiter also wird die Bezeichnung zu modified (soiless) growing mix (MGM) geändert und diese wird auch im weiteren Artikel als korrekte Bezeichnung verwendet.
Bei Indoor living soil spricht man meist von einem Beet oder einem Topfsystem mit mindestens 60-80 Liter Substrat, welches auf Torfbasis mittels Mineralien / organischem Dünger angereichert wird und über mehrere Durchläufe genutzt wird. Hierbei ist das Ziel eine vielfältige und aktive Gemeinschaft von Mikroorganismen zu bilden, darunter Bakterien und Pilze, ergänzt durch nützliche Insekten. Diese Mikroorganismen spielen eine wichtige Rolle für die Gesundheit und das Wachstum der Pflanzen, indem sie wichtige Nährstoffe liefern (Tegeder und Rentsch 2010), die Bodenstruktur verbessern (Rillig und Mummey 2006; Helliwell et al. 2014) und die Widerstandsfähigkeit der Pflanzen gegenüber Schadorganismen (Pathogenen).
Das heißt, es ist zwar in manchen Aspekten sinnvoll die Natur zu imitieren, wie bei dem Schädlingsbeispiel oben, aber auch manchmal ratsam neue Methoden, wie die Verwendung von Torf, zu Nutzen. Unser Ziel ist es bei der Schaffung künstlicher Ökosysteme, den Ertrag/Qualität gegenüber den Inputs zu erhöhen. D.h., unser Ziel bei der Einbringung von neuen Techniken ist es immer, entweder den Output zu erhöhen oder die benötigte Inputmenge (einschließlich Umweltschäden) zu minimieren, um das Verhältnis Output zu Input zu maximieren. Dies sollte immer als oberste Maxime bei der Evaluierung gelten.
Warum das living soil System auch indoor nachhaltig sein kann
Manch einer wird sich nun fragen, ob man mit der ganzen organischen Materie nicht sehr viele Schädlinge einbringt. Diese Frage ist berechtigt und leider trifft dies auch zu.
Jedoch ist dieser Pathogendruck leicht mit einem gut integrierten Pathogen Management System möglich. Dies beinhaltet Prävention durch Reinheit, Nützlings-Insekten und zur Not organischen Spritzmitteln wie Neem-Öl. Das Schädlingsmanagement wird jedoch ein eigener Artikel, da dies den Rahmen des Einführungs-Artikels sprengen würde.
Die Vorteile sind dagegen mannigfaltig. Bei richtigem, lokalem und bewusstem Einkauf von organischen Düngern kann living soil im Vergleich zu anderen Anbau-Methoden pro Durchlauf günstiger und nachhaltiger sein. Es muss jedoch stark darauf geachtet werden, was und wo man kauft, denn oft haben Düngestoffe lange Versandwege oder unethische Raubbau Methoden wie bei bestimmten Guano Herstellern oder Gesteinsmehlen, welche mit Tagewerkabbaumethoden geschürft werden. Dies gilt es zu vermeiden und immer so saisonal und lokal wie möglich einzukaufen, da sonst die Idee mit der Nachhaltigkeit schnell ausgehöhlt wird. Im Optimalfall ist eine LCA (Life cycle assessment) Prüfung für den gesamten Mix vorher durchgeführt worden, diese gibt einen Überblick über sämtliche Externalitäten (Auswirkungen außerhalb des direkten Umfeldes auf das gesamte Ökosystem) der Komponenten. Der später aufgezeigte MGM (modified growing mix) wird CO2 optimiert sein, aber nicht perfekt von Anfang an, sondern auf laufende Verbesserung ausgelegt. Die beste Variante des Mischens ist es, möglichst viele Ausgangsstoffe in den eigenen Kreislauf zu integrieren, also bspw. seinen eigenen Kompost herzustellen, Gesteinsmehle in lokalen Steinbrüchen zu beschaffen und selbst Fermente anzureichern.
Jetzt reden wir von Nachhaltigkeit, aber nutzen Torf als Basis. Warum? Es gibt nachhaltige Abbaupraktiken, welche die CO2-Bilanz, welche durch das ausströmende Methan beim Torfabbau negativ beeinflusst ist, aufbessern und ausgleichen. Es ist darauf zu achten, dass der Betrieb eine Regenerations-Strategie anbietet, denn das reine Ausgleichen der eigenen schlechten CO2-Bilanz bringt dem lokal geschädigten Ökosystem nicht viel.
Ein Beispiel hierfür ist die Veriflora®-Zertifizierung. Es besitzt gute Eigenschaften wie eine geringe Lagerungsdichte (siehe Kapitel 2.1.1) um den Humus auszugleichen, besitzt gute CEC werte (Kapitel 2.2.2) und ist stabil über viele Durchläufe hinweg (Burgel et al. 2020). Dies ist besonders wichtig, wenn man den Boden nicht jedes 3te mal wieder neu anmischen möchte, weil das Substrat zusammensackt. Jedoch kann Torf nicht die reine Grundsubstanz bieten. Welche Zusatzstoffe man benötigt und welche Werte man zur Evaluation nutzt, wird in den folgenden Kapiteln zusammengefasst.
Wieso kann Living Soil leichter eine überlegene Qualität und Expression der Pflanze erzeugen
Das Thema Qualität und seine Definition füllt einen eigenen Artikel, welche nach dieser Artikelreihe erscheinen wird, und deshalb wird hier nur ein kleines Exzerpt aufgezeigt
Das System ist in drei Themengebiete eingeteilt. Die erste Kategorie beschreibt die pharmazeutische Qualität. Die restlichen Bewertungskriterien sind in die grundlegend handwerkliche Herstellung/Verarbeitung und das sensorische Profil aufgespalten. Diese sind in der Abfolge der Hauptkategorien (1.1; 1.2; 1.3) pyramidenartig zu bewerten. Das heißt für ein optimales Produkt müssen diese aufeinander aufbauen erfüllt sein.

Man könnte es mit der Zwei-Faktoren-Theorie von Herzberg vergleichen, wobei hier die pharmazeutische Qualität den Hygienefaktoren und die beiden anderen den Motivationsfaktoren zugeteilt werden kann. (Becker 2019). Das heißt, das Material muss immer mindestens den pharmazeutischen Qualitäten entsprechen bevor man überhaupt daran denken kann, Geschmack oder Blütenverarbeitung zu bewerten. Bei der Gewichtung muss entsprechend zur Marktpositionierung/Stakeholdership der Zieldemografik unterschieden werden bis zu welcher Kategorie Stufe man gehen muss.
Die Grundsteine der pharmazeutischen Definition müssen für die Nutzung von Blüten erfüllt sein. Vor allem im medizinischen Bereich ist die Einhaltung der pharmazeutischen Produktionsstandards eine Grundvoraussetzung. Diese müssen in der gesamten Wertschöpfungskette von Anzucht bis hin zur Verpackung eingehalten werden.
Von GACP über EU-cGxP bis hin zu HACCP Richtlinien und den weiterführenden Zertifizierungen gibt es viele Wege die Vorgaben des europäischen Zentrallabors zu erfüllen und zu übertreffen. Diese beziehen sich auf die grundlegenden Testkriterien nach dem Deutschen Arzneibuchs (DAB) welche sich aus Reinheit, Identität und Wirkstoffgehalt zusammensetzen. Umgangssprachlich bedeutet dies: Ist die Blüte frei von Pestiziden, Schwermetallen und mikrobieller Belastung; ist es wirklich Cannabis und ist so viel Wirkstoff enthalten wie angegeben (Deutscher Apotheker Verlag 2021).
Ob man allerdings für die Einhaltung dieser Grundqualitäten unbedingt GACP/GMP benötigt, sei dahingestellt, mein Kollege Lorenz hat sich bereits tiefer mit diesem Thema befasst. Es sei nur gesagt, man kann auch ohne eine 100 Mio. EUR Anlage hochwertige, reine Produkte schaffen.
Diese Qualitätsstufe ist leicht mit Living soil abdeckbar, man muss nur dass Mikrobenkonsortium beachten (Kapitel 2.3) und mit pharmazeutischer Reinheit arbeiten also keine Sprays in Blüte, nur mit Bart/Haarnetzen / Handschuhen arbeiten und Blütentests (COAs – Certificates of analysis) einreichen.
Die zweite Qualitätsstufe ist die handwerkliche Qualität. Handwerkliche Qualitäten umfassen Faktoren, welche objektiv bei Endprodukten bewertet, werden können und im Herstellungsprozess enthalten sind. Dazu gehören
- Der Kultivar (Ahnenbaum und Güte der Selektion)
- Der Anbau (Expression des Kultivars, Nachhaltigkeit)
- Die Trocknung
- Trim, Behandlung und Lagerung des Materials
- Konsumenteneigne Bewertungen wie „White ash“
Insbesondere der Anbau ist hier natürlich der ausschlaggebende Faktor. Und hierunter die Expression des Kultivars, welche die Ausprägung des genetischen Basismaterials unter Einwirkung des Growers und der Umwelt entsteht. Sozusagen ein Miniterroir, wenn sich jemand mit Wein befasst. Es beschreibt nicht, dass einem das Geruchsprofil persönlich gefällt, sondern, dass der Cut gut ausgegrowt wurde.
Beispiel Haze: viele Leute hassen Haze, aber ein gut gegrowtes Haze, bleibt handwerkliche gesehen doch ein gutes Haze, wenn es seine vollen 15 Wochen gehen darf und feine, tiefgehende Noten besitzt. Es stellt also seine eigenen Besonderheiten in den Vordergrund. Die Genetik und die Güte ihrer Selektion kommt hier offensichtlich als begrenzender Faktor, da eine spezifischer Kultivar nur so gut gegrowt werden kann, wie es genetisch vermag. Daher steht am Anfang jedes überlegenen Produktes eine intensive Selektion, um dann die möglichst beste Expression herauszukitzeln (Dial in Prozess)
Dies ist mit allen Anbaumethoden möglich, jedoch schneller und einfacher mit Living Soil, denn dieser ermöglicht er der Pflanze selbst zu entscheiden, welche Nährstoffe aufgenommen werden und wann sie damit stoppen muss z.B. um ein optimales Ausreifen/Seneszenz zu erreichen, genaueres in Kapitel 2.2.3 Die Aufnahme der Nährstoffe an den Wurzeln. Um dies zu erreichen, muss natürlich das Handwerkzeug sitzen, deshalb fällt die Bewertung dieser Kriterien auch unter die handwerkliche Qualität.
Die finale Ebene der Qualität ist dann eher subjektiv und in ihrer Bewertung oft von den Testern abhängig da sie die sensorische Qualität bewertet. Zwar kann man diese auch in Messwerte wie Terpenkonzentration, Diversität oder THC-Messwerte eingeteilt werden, dies wird meiner Meinung aber den delikaten Unterschieden der Blüte nicht gerecht und basiert auf dem Ansatz der Wissenschaft alles runterzubrechen. Ich bin mehr als viele andere ein vehementer Vertreter der Wissenschaft, aber bei Genußmitteln wie Wein, Zigarre, Spiritousen oder eben auch Cannabis sehe ich den Mensch immer noch im Voraus. Deshalb würde ich ein Bewertungssystem wie die Robert-Parker Punkte für Wein für sensorische und gesamte Qualität gegenüber den Messwertbezogenen aktuellen Systemen vorziehen.
Gelernte Assessoren trainieren jahrelang für diese Jobs, daher ist es nicht ganz so leicht diese Fähigkeit zu erhalten. Insbesondere im Graubereich von Cannabis, wo auch noch intensive Black market Tätigkeit von Nöten ist. Dies ist einer unserer Vorteile als non-legal market Teilnehmer gegenüber der neuen Leute, die sich jetzt alle auf einmal einschleichen, sobald es legal wird. Es wird also hoffentlich immer einen Platz für Leute mit Sinn für Qualität geben.
Ein lebendes, organisches System kann auch hier wieder von Vorteil sein, da durch die Zerfallsprozesse im Boden hunderte Abbauprodukte wie Capronsäure oder kohlenstoffbasierte Nährstoffe entstehen, welche der Pflanze ganz andere Möglichkeiten gibt, um Energie zu sparen und zusätzliche Abwehrstoffe zu bilden, hinter welchen wir ja bei Cannabis spezifisch hinterher sind. Es gibt nämlich auch Stoffe wie Laktone, welche in winzigen Mengen vorliegen, welche in den meisten Tests nicht aufgeschlüsselt werden und trotzdem einen signifikanten Einfluss auf das Geruchsprofil haben. Dies kann man ganz klar sehen, wenn man Cannabis basierte und synthetisch basierte Terpenmischung für z.B. Cartridges vergleicht. Dieser Wert wird in n-butanol Referenzwerten angegeben.
Abbildung 1: Einordnungsskala Geruchsintensität im Vergleich zu n-Butanol (St. Croix Sensory Inc. 2018)
Zusammenfassend kann man sagen Living soil macht es leichter eine optimale Expression des Kultivars zu schaffen und das maximale genetische Potential zu erreichen. Damit erleichtert er die Qualitätsstufen 2/3, die erste Stufe (pharmazeutische Qualität) ist allerdings etwas schwieriger zu erreichen als bei einem inerten Steinwollsystem, da diese deutlich leichter rein zu halten sind.
Eine exakte Auflistung und ein integratives Bewertungssystem der aktuellen Qualitätsdefinition folgt im Artikel: "Was macht Cannabis Qualität aus".
Wie setzt sich ein guter Boden zusammen
Doch was muss ich nun alles beachten beim Zusammenstellen? Dafür müssen wir uns zunächst den „optimalen“ MGM ansehen. Diesen einen gibt es nämlich nicht, denn jede Situation, jedes Setup und jeder Growstyle ist anders. Darum muss man sich die Werkzeuge und Stellschrauben zusammenschreiben und dann situationsbedingt den Soilmix anpassen.
Hat man z.B. einen Grow mit maximaler Bestrahlung (1200umol/s*m2), aber kein Gießsystem mit Sensor, ist ein Boden mit hoher Feldkapazität (Wasserhaltekapazität) von Vorteil. Möchte man mehr kurzfristige Kontrolle und kann oft nachdüngen, ist die Verwendung von schnell verfügbaren Düngemitteln in geringerer Konzentration vorteilhafter als einmal eine große, langsam verfügbar werdende Menge an organischem Dünger zu verwenden.
Doch solche Strategien kommen später, dafür müssen erst die Grundlagen sitzen. Dafür klären wir zunächst die wichtigsten Begriffe zum Thema, welche im indoor living soil wichtig sind. Dies wird keinesfalls vollumfänglich sein, insbesondere von wissenschaftlicher Seite. Ich empfehle hierfür das Buch (Blume et al. 2010) für einen vollumfänglichen Überblick der Bodenkunde.
Physikalische Faktoren
Lagerungsdichte, Körnung und Aggregation
Die Lagerungsdichte ist ein Maß für die Masse des Bodens in einem bestimmten Volumen. Sie wird normalerweise in Gramm pro Kubikzentimeter (g/cm^3) oder Pfund pro Kubikfuß (lb/ft^3) angegeben. Die Lagerungsdichte des Bodens ist eine wichtige physikalische Eigenschaft, die sich auf die Fähigkeit des Bodens auswirken kann, das Pflanzenwachstum und die Bewegung von Wasser und Nährstoffen durch den Boden zu unterstützen.
Es gibt mehrere Faktoren, die die Lagerungsdichte des Bodens beeinflussen können, darunter die Art des Bodens, die Art und Menge der vorhandenen organischen Substanz sowie die Zusammensetzung des Porenprofils. Böden mit einem hohen Anteil an organischer Substanz haben tendenziell eine geringere Lagerungsdichte, da die organische Substanz Raum einnimmt und die Dichte des Bodens verringert, dies gilt für richtige Böden mit Lehm, in unserem Torfbasierten System ist die Dichte ziemlich gleich zum Ausgangsmaterial Torf. Ebenso haben Böden mit einem hohen Anteil an Poren tendenziell eine geringere Lagerungsdichte, da die Poren Hohlräume bilden, die nicht mit Bodenteilchen gefüllt sind.
Die Lagerungsdichte kann auch durch Bodenbewirtschaftungsmethoden beeinflusst werden. So kann beispielsweise die Bearbeitung des Bodens mit schweren Maschinen oder grobem Umgraben, welches die natürlichen Aggregrate aufbricht, die Lagerungsdichte erhöhen.
Das Verständnis der Lagerungsdichte des Bodens kann für eine Reihe von Zwecken nützlich sein. In der Landwirtschaft beispielsweise kann die Kenntnis der Lagerungsdichte des Bodens den Landwirten helfen, Bewässerungs- und Düngeverfahren zu optimieren. Sie kann auch zur Vorhersage der Bewegung von Wasser und gelösten Stoffen durch den Boden verwendet werden, was für die Vorhersage des Risikos der Bodenerosion und der Auswaschung von Schadstoffen wichtig sein kann. Doch um Implikationen für den Anbau herauslesen zu können, benötigen wir noch mehr Angaben wie Körnung, Porenzusammensetzung, Aggregation und die Zielwerte.
Als Körnung bezeichnet man als die Zusammensetzung der Mineralkörper aus primären/sekundären Mineralien also z.B. Bimsstein oder Silikaten im Boden. Von Aggregaten spricht man, wenn sich diese Körner oder organische Teilchen wie beim Torf zusammen einen Komplex bilden. Wenn ihr schonmal Gartenerde aufgemacht habt, wisst ihr was ich meine, das ist ja auch nicht perfekt homogenes Pulver, sondern sollte eine schöne Krümelstruktur aufweist. Diese „Stückchen“ im Boden sind Zusammensetzungen von organischer Materie, Microbiom (Bakterienschleim), Mineralien und Porenverteilung ab.
Abbildung 2: Schwarztorf, das Substrat mit fast perfekter Struktur (International Peatland Society 2019)
Im Cannabisanbau spezifisch sind Forscher gerade dabei zu ermitteln, welches die optimalen Werte für Lagerungsdichte / Zusammensetzung sind, jedoch gibt es im Anbau selbst bisher leider wenig Daten. Diese sind oft schwer ermittelbar für living soil Substratmischungen, da sowohl die Mischungsverhältnisse als auch die Mikrobielle Zusammensetzung inhomogen sind.
Nach eigenen Versuchen und Beratung durch Jonathan Traxler würde ich eine Dichte von 0.4-5g/cm3 oder 400-500kg/m3 empfehlen, dies ist aber auch wieder abhängig von der Zielsetzung, wir haben diesen Wert genommen, um die Porenbalance zu den Mittelporen zu verschieben, um Gehalte in Sauerstoff und Wasserhaltefähigkeit zu maximieren und gleichzeitig den Boden schwer genug zu machen, um eine entsprechend hohe Totale Austauschkapazität zu schaffen.
Diese Begriffe und Qualitätsmerkmale werden im nächsten Kapitel und im Kapitel 2.2.4 CEC und AEC – Kationen und Anionen Austausch Kapazität und Basissättigung erklärt.
Für die einfache Heimanwendung reicht eine optische Bewertung der Struktur/Aggregation indem man eine Handvoll nimmt, diese bis zur Sättigung anfeuchtet und zusammendrückt. Es sollte leicht tropfen und einen „losen“ Klumpen bilden, welcher sich aber nach kurzer Zeit wieder auseinander bewegt. Man kann auch den Boden selbst leicht mit der Hand aufgraben und sehen, wie groß die Bodenaggregate sind. Es sollten knapp 3-4cm3 Aggregate/Klumpen sein, dies wird auch als Krümelstruktur bezeichnet.
Es gibt Studien wie (Campbell et al. 2021), welche sich Substrateinfluss unter Nutzung von mineralischen Nährstoffen und Hormonen auf die Bewurzelung von Stecklingen anschauen. Hier gibt es eine reine Versuchsreihe zum Einfluss von Substraten auf die Wurzelrate und das Wurzelgewicht. Alle Parameter wurden positiv von geringer Lagerungsdichte und höherer Porosität bis zu einem gewissen Punkt beeinflusst. Zu hohe Porosität in der Hinsicht, dass ein mangelnder Kontakt zwischen Wurzeln und Erde besteht, führt zum Verlust des Turgors, dem inneren Wasserdruck, der die Pflanze aufrecht hält. (LOACH 1985)
Porengröße und Verteilung
Poren sind die Zwischenräumen der Körner und ergeben sich aus deren Größe /Lagerung, welche wir im letzten Kapitel betrachtet haben. Sie spielen eine entscheidende Rolle für die physikalischen und chemischen Eigenschaften des Bodens, da sie deren Fähigkeit, Wasser, Luft und andere Stoffe aufzunehmen, beeinflussen können.
Die Porengröße bezieht sich auf den Durchmesser der Öffnungen in einem Material. Die Größe der Poren kann von klein, wie z. B. in Lehmboden, bis zu sehr viel größer, wie z. B. in Sand, reichen. Die Größe der Poren in einem Material kann einen erheblichen Einfluss auf seine Eigenschaften haben.
Mit abnehmendem Porendurchmesser wird das Wasser fester in diesen Poren gebunden. Je kleiner der Porendurchmesser, umso höher ist die Saugspannung (in cm Wassersäule "WS"), mit der das Wasser, entsprechend den Bedingungen in einer feinen Kapillare, festgehalten wird. Der pF-Wert (=log cm WS) beschreibt die Wasserbindung im Boden in anschaulicher Form. Je höher der pF Wert, desto mehr „Kraft“ benötigt es, um das Wasser aus den Poren zu entfernen. Referenzwerte hierfür gibt es in Abbildung 1: Porenverteilung (Blume et al., 2010). Der pF-Wert kann in kPA, mbar und andere Spannungseinheiten umgerechnet werden.
Sehr feine Poren können z.B. nur unter Zuhilfenahme von starkem Unterdruck oder Hitze geleert werden. Dieses Phenomän ist unteranderem mitverantwortlich, dass Mikroorganismen sich selbst bei stärkster Austrocknung im Boden sicher einlagern können (Sporulation bleibt trotzdem der Ausschlaggebende Faktor beim Überleben der Mikroorganismen).
In der Tabelle sehen wir die Verteilung der Poren. Man kann die Grobporen weiterhin in weite und enge Grobporen unterteilen. Zwischen 10-50mm bezeichnet man sie als eng und >50mm dann als weite Grobporen. Die Engen verhalten sich mehr wie Mittelporen und sind eine gute Mischung aus Drainage und Wasserhaltung. Über 50mm fungiert es mehr als reine Drainage Poren, da kein Wasser gegen die Schwerkraft gehalten werden kann.
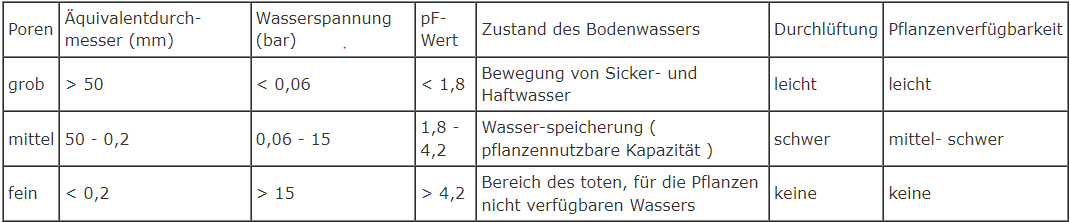
Abbildung 3: Porenverteilung (Blume et al. 2010)
Eine wichtige Funktion der Poren ist ihre Rolle bei der Wasserspeicherung. Poren, die groß genug sind, um Wasser zu halten, aber nicht so groß, dass das Wasser schnell abfließt, werden als "effektive Poren" oder Mittelporen bezeichnet. Materialien mit einem hohen Anteil an effektiven Poren sind in der Lage, mehr Wasser zu speichern und es über einen längeren Zeitraum zurückzuhalten. Dies kann in Gebieten mit geringen Niederschlägen oder Trockenheit von Vorteil sein.
Poren spielen auch eine Rolle beim Austausch von Gasen, wie Sauerstoff und Kohlendioxid. In Böden beispielsweise sind Poren wichtig für die Luftbewegung und den Austausch von Gasen zwischen dem Boden und der Atmosphäre. Dies ist für das Wachstum und die Gesundheit von Pflanzen von entscheidender Bedeutung, da sie für die Atmung und die Aufnahme von Nährstoffen auf die Zufuhr von Sauerstoff angewiesen sind.
Aus diesem Grund muss wie eingangs erwähnt auch wieder auf den jeweiligen Anwendungsfall geachtet werden. Dieser bestimmt, ob man mehr Drainage oder mehr Wasserhaltefähigkeit benötigt, und je nachdem muss man bestimmt Mischverhältnisse bei den Bodensubstanzen einhalten, um entsprechende Verteilungen an Poren zu erhalten. Das Ziel ist es immer ungefähr das Profil von Torf zu erhalten, d.h. wenn ich jetzt sehr dichte Materialen wie Biochar oder Lehm/Kompostmischung hinzugebe, muss ich im selben Maße Belüftungsmaterialien hinzugeben, um die Balance zu erhalten.
Unser Grundstoff Torf besitzt hervorragende Eigenschaften für eine Vielzahl von Anwendungen. Die Porenverteilung zeigt besonders bei den Mittelporen einen linksseitigen Ausschlag. Das heißt der größte Volumenanteil der Poren befindet sich im pflanzenverfügbaren Bereich. Vorallem der Schwarztorf ( c ) eignet sich hierfür hervorragend.

Abbildung 4: Porengrößenverteilung verschiedener Torfarten (Turunen et al. 2019)
Feldkapazität und Bewässerung
Ohne Wasser, kein gesunder Boden. Ohne das richtige Gießverhalten können die Abbauprozesse und die Nährstoffversorgung der Pflanze nicht aufrechterhalten werden. Zudem könnt ihr euren Boden permanent schädigen, wenn ihr ihn zu lange trocknen lasst.
Ein wichtiger Begriff ist die Feldkapazität (FK). Sie entspricht dem Wasservolumen der auf pF 1,8 (=60 cm Wassersäule) entwässerten bzw. bei entsprechender Feuchte entnommenen Bodenproben. Dies heißt mehr oder weniger wieviel gesamtverfügbares Wasser im Boden gegen die Schwerkraft in den Poren gehalten werden kann also unser maximal verfügbarer Wasserspeicher.
Entsprechend der Einteilung der Porengrößen bezeichnet man den Porenbereich von 0,2 mm bis 50 mm als die nutzbare Feldkapazität (nFK) eines Bodens, da das enthaltene Porenwasser pflanzenverfügbar ist. Das Wasser der Poren < 0,2 mm ist nicht mehr pflanzenverfügbar und wird deshalb als "Totwasser" bezeichnet, da es zu hohe Saugkraft von der Pflanze benötigen würde, um verwendet zu werden. Es wird bei der Berechnung von nFK rausgerechnet. Der sog. permanente Welkepunkt (PWP) liegt bei pF 4,2 oder 1000kPA. (Blume et al. 2010). Um das ganze etwas anschaulicher zu machen, schaut ihr euch am besten dieses Video
Wird der PWP während der Kultur erreicht, stirbt die Pflanze ab. Allerdings ist der Punkt, ab dem die Welke beginnt bei verschiedenen Pflanzen unterschiedlich. So ist Cannabis s. tolerant und kann bis zu hohen pF-Werten zurücktrocknen ohne zu sterbe. Dies sollte jedoch nur genutzt werden, um gezielt Stressstimulationen zu applizieren, da dauerhaft Dürre einen verminderten Ertrag bedeutet.
Je nachdem wieviel % nFK wir im Boden gefüllt haben, gibt es einen unterschiedlich starken Saugdruck bzw. eine Saugspannung auf die Wurzel. Je trockener der Boden, desto mehr Kraft muss die Pflanze aufwenden, um das Wasser aufnehmen zu können.
Diese Saugstärke kann man mit einem Tensiometer messen und wird in der Bodenkunde als Matrixpotential bezeichnet. Das Matrixpotential wird in mbar oder kPA gemessen. Da bisher wenig Forschung dazu betrieben wurden / es wenig etablierte Werte gibt für Torf, muss man auf Erfahrungswerte und annekdotische Beweise zurückgreifen. Diese stammen entweder von Anwendern aus den Foren oder aus Podcasts wie „Cannabis science and cultivation“ by Tad Hussey. Ein Beispiel ist eine Episode vom
Die bis her festgestellten optimalen Werte sind auch von Kultivar zu Kultivar unterschiedlich und müssen final vom Grower selbst anhand seiner Einschätzung zur Vitalität der Pflanze festgelegt werden. Je niedriger die Saugspannung desto gesättigter ist der Boden mit Wasser. In den Werten können wir sehen, dass wir die vegetative Phase nasser fahren als z.B. in gewollten Stressperioden wie der Flower I oder Flower III Phase in denen wir gezielt leichten Trockenstress induzieren wollen.
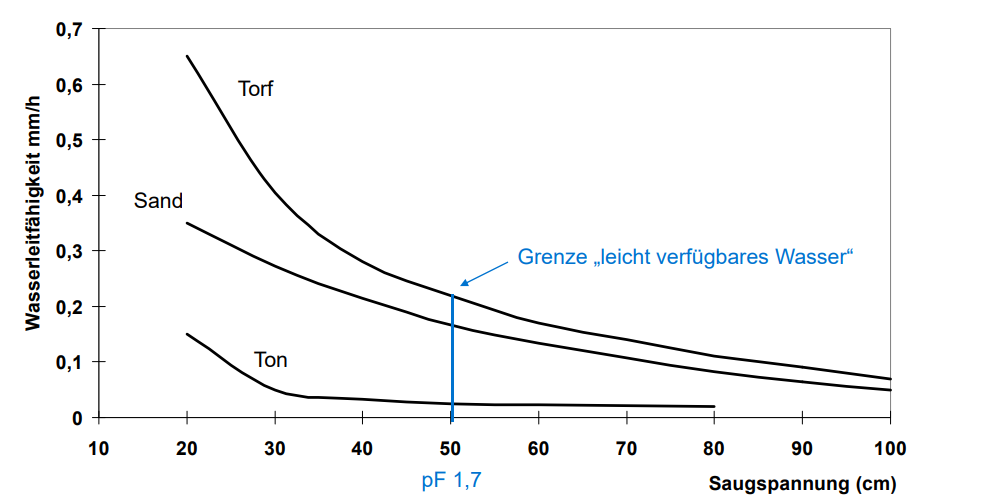
Abbildung 5: Wasserhaltefähigkeit unter Saugspannung
Der Stress sollte aber nur angewandt werden, wenn volle Kontrolle über das System und die Pflanze besteht, denn wenn die Pflanze eh schon gestresst ist, wollen wir nicht unnötig mehr applizieren. (Geelen et al. 2019)
Es gibt Wege diesen Stress zu quantifizieren, dies erfordert jedoch aufwendiges Forschungsgerät und sind nicht für den Heimnutzer geeignet. Für kommerzielle Kultivierungsbetriebe lohnt sich dies wiederum enorm zur Etablierung von Kultivierung SOPs der einzelnen Kultivare. Es benötigt hierfür aber einen Forschungsleiter bzw. einen Berater, der sich hierbei auskennt.
Hier sind bisher von mir und der Szene ermittelte Richtwerte für die Saugspannung in Indoor, torfbasierten Living soil Systemen:
| Lebensphase | Beginn Veg | Mitte | Ende Veg | Flower I: Übergang |
Flower II: Bulk | Flower III:
Reifung |
| Mbar Range | 40-50 | 40-60 | 40-80 | 120-160 | 60-100 | 120-160 |
Tabelle 1: Referenzwerte Saugspannung zur Bewässerung
Um den Sättigungsgrad optimal steuern zu können, braucht ihr ein gutes Tensiometer wie oben bereits erwähnt. Das Beste nicht rein kommerziell erwerbbare ist das Irrometer SR, welches für leichte Böden, wie unsere Torfmischungen, geeignet ist. Es gibt auch Varianten mit digitalem Ausgang, welche man in eine Bewässerungssteuerung einbauen kann, aber dies im Detail zu zeigen, würde wieder den Rahmen sprengen.
Günstige Alternativen dazu findet ihr bei Blumat oder ähnlichen Herstellern. Diese gilt es auf ca. 30cm je nach Tiefe des Beets einzusetzen. Am besten nehmt ihr die Mitte des Beets, aber messt auch in regelmäßigen Intervallen das komplette Beet ab, um evtl. inhomogene Wasserverteilung festzustellen und euer Gießverhalten anzupassen. Wenn man nun einen sehr fancy/high tech Begriff verwenden möchte, könnte man dieses Gießverhalten als organic crop steering bezeichnen, obwohl dieses auch noch die Steuerung der Umwelt eigentlich mit einbezieht. Es ist die Königsdisziplin und wir im Kapitel 4. Vorgehensweise und Zeitplan bei der Verwendung von Living soil besprochen.
Chemische Faktoren
Da wir nun die physikalischen Eigenschaften weitestgehenden betrachtet haben, wenden wir uns den chemischen Eigenschaften des Bodens und der Pflanzenernährung zu. Zunächst ein Überblick über die 16 Nährstoffe die es für einen produktiven Lebenszyklus in Pflanzen benötigt, dann der pH-Wert im Fokus, gefolgt vom Ausnahmeprinzip der Nährstoffe an der Wurzel und abschließend eine Erläuterung des Ionen Austauschsprinzip an Oberflächen.
Pflanzennährstoffe 101
Wie alle Pflanzen benötigt auch Cannabis ein ausgewogenes Verhältnis von Makro- und Mikronährstoffen, um richtig zu wachsen und sich zu entwickeln. Makro- und Mikronährstoffe werden für eine Vielzahl von Pflanzenprozessen benötigt, darunter die Photosynthese, die Proteinsynthese und die Funktion von Enzymen. Ich empfehle (Maathuis und Diatloff 2013; Pandey 2018) als Reviews zum Thema mit tiefgehenden physiologischen Erklärungen.
Für detaillierte Informationen über Pflanzennährstoffe spezifisch für Cannabis ist die Forschung von Dr. Nitrit Bernstein, (Llewellyn et al. 2023) und (Cockson et al. 2019b) empfohlen oder für praktische Videos zum Thema, den YouTube-Kanal von Greengenesgarden
Referenzwerte, Anwendungshinweise und empfohlene Konzentrationen der Nährstoffe kommen im Kapitel“3. Wie teste ich dies Bestandteile meines Bodensystems“, da es einige verschiedene Stellschrauben gibt und man diese erst noch kennen muss, um damit etwas anfangen zu können.
Makronährstoffe
Es gibt 6 wichtige Makronährstoffe, die Cannabispflanzen für ihr Wachstum und ihre Entwicklung benötigen. Dazu gehören Stickstoff (N), Phosphor (P), Kalium (K), Kalzium (Ca), Magnesium (Mg) und Schwefel (S), welche mit mindestens 150g/kg Pflanzenmaterial trocken benötigt werden und deswegen auch Makronährstoffe genannt werden.
Stickstoff
Zunächst zum wichtigsten Bestandteile, da er die Basis für jegliche Proteinproduktion in der Pflanze ist, welche die funktionalsten Moleküle der Pflanze ausmachen. Es ist also integral für das Wachstum und die Biomasse. Er ist auch Bestandteil der Nukleinsäuren (Adenin, Guanin, Cytosin, Thymin und Uracil), welche die Basis der DNA-Information bilden und wird für die Produktion von Chlorophyll benötigt, welches das funktionelle Organell der Photosynthese ist. (Pandey 2018)

Abbildung 6: Stickstoffformen und deren Verwendung in der Pflanze (Pandey 2018)
Enthalten ist der Stoff in den meisten Chlorophyll enthaltenden Geweben von Pflanzen und in jeglichen Aminosäuren basierten Stoffe wie Peptiden/Proteinen aus z.B. Blut/Horn/Soja. Es gibt eine Vielzahl an organischen Gebinden, welche Stickstoff in sich tragen, jedoch wird das meiste in Form von Rottkomposten oder Wurmkomposten in den Boden eingebracht.
Diese organisch gebundenen Formen wie Huminsäure (C9H9NO6) sind komplex und vielfältig also wäre eine genaue Auflistung zu viel, es wird aber eine Amendmentliste noch in Kapitel 2.4.5 geben.
Wenn diese Stoffe durch Mikroben verdaut oder durch chemische Interaktion mineralisiert/verfügbar gemacht werden, liegen sie zum Großteil als Ammonium (NH4+) oder Nitrat (NO3-) vor. Einjährige Pflanzen wie Cannabis s. weisen eine Ammoniumunverträglichkeit ab einer gewissen, Kultivarspezifischen Konzentration auf (Esteban et al. 2016). Bis zu dieser Konzentration kann es aber von Vorteil sein einen Teil des Stickstoffs über NH4+ zu supplementieren, denn wie man in Abbildung 4: Stickstoffaufnahme und Verwertung in der Pflanze (Li et al., 2017) sieht, spart dies wieder einen Syntheseschritt und somit Energie / ATP, welche die Pflanze nicht aufwenden muss.
In dieser Abbildung sieht man auch nochmals den Vorteil der direkten Aminosäuren Applikation, denn diese können direkt in Glumatinsäure verarbeitet werden und als Basis für die folgenden Syntheseschritte genutzt werden. (Pandey 2018)
Abbildung 7: Stickstoffaufnahme und Verwertung in der Pflanze (Li et al. 2017)
Phosphor
Ein weiterer wichtiger Makronährstoff für Cannabispflanzen ist Phosphor. Er wird sowohl für die Synthese von DNA und RNA als auch für die Erzeugung von Energie in Form von ATP (Adenosintriphosphat) benötigt. Das heißt es ist sowohl in jeder Zelle als Zellvorlage enthalten als auch Basis für jegliche Endenergiequelle der Zelle und gilt als Währung für jeden Prozess der in der Pflanze abläuft. (Pandey 2018)
Desweiteren ist es der wichtigste Bestandteil der Membranen, denn diese sind buchstäblich Phosphor Doppelschichten, ein Beispiel ist der casparische Streifen, welcher als Abscheider und Filter in den Wurzeln fungiert. Sie sind auch zusammen mit Calcium das wichtigste Biomineral in Trichomen und zu einem Teil durch ihre weißen Rückstände bei der Verbrennung für „white ash“ verantwortlich. (Weigend et al. 2018)
Abbildung 8: Mineralische Zusammensetzung Pflanzentrichome (Weigend et al. 2018)
Es wird zum Großteil als H2PO4- aufgenommen und liegt im Boden entweder als inorganischer, reiner Phosphor oder organophosphorische Form vor. Als Amendments verwendet man hauptsächlich Gesteinsphosphate wie weicherdiges Rohphosphat oder tierische Produkte wie Dung, Guano oder Knochenmehl. (Pandey 2018)
Ein Mangel resultiert in verringerter photosynthetischer Aktivität und damit mit verringerter Leistungsfähigkeit und geringerer Aktivität verschiedener Coenzyme einher, was die Pflanze anfällig für biotischen und abiotischen Stress macht. Es gibt noch wenige Studien, die wirkliche Lebensphasen spezifische Analysen für Nährstoffe machen, jedoch kann aus anekdotischer Erfahrung heraus gesagt werden, da P insbesondere zu Beginn der Blütephase (stretch) eine entscheidende Rolle spielt. Im späteren Verlauf, also ab der Bulkphase (Woche 3-6) übernimmt dann Kalium als tragender Nährstoff. Beide handeln im Zusammenspiel mit Calcium.
Kalium
Aufgrund der hohen Durchlässigkeit der Pflanzenmembranen für K+ nehmen die Pflanzen Kalium schnell auf. Es zeichnet sich durch eine hohe Mobilität in der Pflanze aus und wird in jüngeres Gewebe verlagert.
Eine enge Beziehung zwischen den Wasserkanälen und den Kanälen für die Kaliumaufnahme trägt zur Aufrechterhaltung der pflanzlichen Homöostase bei, diesen Aufnahmemechanismus wird in Kapitel 2.2.3 genauer beleuchtet.
Es ist im Zytoplasma weit verbreitet und dient der Aufrechterhaltung des Ionengleichgewichts und der Osmoregulation in Pflanzenzellen durch Neutralisierung unlöslicher makromolekularer Anionen. Seine hohe Konzentration in den Zellvakuolen fördert die turgorgesteuerte Entwicklung der Zellstreckung, dies wird z.B. auch bei den Wächterzellen der Stomata eingesetzt. Diese werden über Ionenkanäle mit K+ vollgepumpt und durch die Osmose wandert dann das Wasser nach, wodurch sich die Wächterzellen öffnen.
Kaliummangel verringert den Turgor und die Zellgröße, was zu einer verringerten Blattfläche und Stammverlängerung führt. Der Mangel schädigt zudem die Zell innere pH Regulation und beeinträchtigt die Aktivität von über 50 Enzymen, was auch wieder in einer Anfälligkeit für biotischen und abiotischen Stress endet.
Schwefel schützt über Phytochelatine zudem vor gefährlichen Schwermetallablagerungen. Überschüssige Schwermetalle induzieren die Expression von Phytochelatinsynthase, die die Herstellung der als Phytochelatine bekannten Polypeptide mit niedrigem Molekulargewicht aus Glutathion katalysiert.
Supplementiert wird dieser Stoff hauptsächlich über Rottkomposte, Wurmkomposte und Mineralien wie Langbeinit. Im KNF werden Wasserauszüge von Kalium anreichernden Pflanzen wie Tabak verwendet also direkte Zugabe des Kaliums.
Kalzium
Calcium kommt im Pflanzengewebe als Ca2+, Ca-Carbonat, Ca-Phosphat und Ca-Oxalat vor. Welche dieser Formen im Boden sich anreichern ist von immenser Bedeutung, da z.B. eine Anreicherung von bi carbonaten im Boden die meisten Nährstoffe unlöslich macht und somit nicht verfügbar für die Pflanze. Die Aufnahme von Ca2+ ist langsam, da es nur von unreifen Wurzelspitzen absorbiert wird. Es ist essenziell für die Wurzelbildung, wie man in der Abbildung sehen kann, hier orientiert sich die Wurzel anhand des Kalziumgradientens. (Pandey 2018)
Abbildung 9: Kalziumabhängiges Wurzelwachstum (Carol und Dolan 2002)
Die Aufnahme ist ein passiver Prozess, der durch die Anwesenheit von K+, Mg2+ und NH4+ gehemmt wird. Im Zytoplasma wird eine geringe Menge an Kalzium aufrechterhalten, um ungünstige Wechselwirkungen mit anderen Nährstoffionen (PO4, Mg2+) und die Deaktivierung von Enzymen zu vermeiden. Es wird auch benötigt, damit es als zweiter Botenstoff dienen kann. Die niedrige Kalziumkonzentration im Zytoplasma (0,2 M) wird durch die Kontrolle des Ca2+-Flusses durch die zellulären und subzellulären Membranen aufrechterhalten. (Pandey 2018)
Membranenintegrität und somit die Widerstandsfähigkeit der Zellwände hängt direkt von der Calciumkonzentration ab. Auch die Callose, welche als Virenbekämpfungsmaßnahme an den Zellverbindungsschächten (Plasmodesmata) angereichert wird, basiert auf Calcium. Dies blockiert einen der Verbreitungswege von Viren/Viroiden zwischen den Pflanzenzellen.
Eine aktuelle entdeckung ist Rolle von Ca2+ als Signalübertragungsmolekül. Die Wahrnehmung von Stresssignalen führt dazu, dass sich Kalziumkanäle kurzzeitig öffnen und Kalzium in das Zytoplasma gepumpt wird, wodurch sich seine zytosolische Konzentration erhöht. Was dann Abwehrmechanismen im Rahmen der PTI (Pattern triggered immunity/Muster assoziierte/getriggerte Immunität)
Es ist ein immobiler Nährstoff und muss somit im Gießwasser von der Pflanze durch das Xylem Bahnen System an die Spitze der Pflanze transportiert werden. Mängel zeigen sich das zuerst an den Spitzen.
Magnesium
Magnesium wird in deutlich geringeren Mengen benötigt also andere Kationen wie Calcium. Dies könnte auf eine hohe Kationen-Konkurrenz bei der Absorption und einen Mangel an Magnesiumtransportern im Plasmalemma zurückzuführen sein. Ein niedriger pH-Wert und Kationen wie K+, NH4+, Ca2+ und Mn2+ hemmen die Mg2+-Absorption. Die Absorptionsrate ist langsam.
Magnesium hat mehrere verschiedene Funktionen. Die Mobilität des Magnesiums in den Zellen ist mit seiner Funktion verbunden. Die Hauptfunktion des Magnesiums ergibt sich aus seiner Position als Kernelement des Chlorophyllmoleküls. Dieses Organell ist der Grundstein der Photosynthese und wenn das Zentralatom fehlt, ist logischerweise auch die Photosynthese Leistung stark beeinträchtigt (Pandey 2018).
Typische Amendments zur Magnesiumversorgung sind Algenkalk oder Epsomsalz (MgSO4-), welches noch nützlicherweise Schwefel enthält. Je nach Ökoverband muss allerdings bei dem Gebrauch von Sulfaten aufgepasst werden, da diese teilweise als „böse“ mineralische Düngestoffe gewertet werden.
Schwefel
Schwefel liegt als SO4- also Sulphat vor, die typischsten Formen sind Gips (Calcium sulfat), welcher zusätzlich ein exzellenter, pH-neutrales Calciumlieferant ist und organische Verbindungen wie z.B. in Komposten.
Die Sulfidreduktion im Rahmen des Stoffwechsels der Pflanze führt zum Einbau von Sulfid in eine Vielzahl verschiedener Moleküle, darunter die Aminosäuren Cystein und Methionin, Coenzyme und Sekundärmetaboliten. Cystein und Methionin sind beide wesentliche Bestandteile von Pflanzenproteinen. Diese Aminosäuren sind besonders wichtig, weil Tiere und Menschen nicht in der Lage sind, Schwefel abzubauen, und zur Deckung ihres Nährstoffbedarfs auf Pflanzen angewiesen sind. Darum ist eine adäquate Schwefelversorgung bei jeder Pflanze wichtig. Auch das wichtigste Entgiftungsenzym Glutathion basiert auf Schwefelverbindungen (Cystein) (Pandey 2018)
Schwefel schützt über Phytochelatine vor gefährlichen Schwermetallablagerungen. Überschüssige Schwermetalle induzieren die Expression von Phytochelatinsynthase, die die Herstellung der als Phytochelatine bekannten Polypeptide mit niedrigem Molekulargewicht aus Glutathion katalysiert. (Pandey 2018)
Bei Cannabis ist besonders der Punkt der erhöhten Sekundärmetabolit Synthese von Bedeutung, da diese besonders die VSC (volatile Sulfur Compounds/volatile Schwefelstoffe) Anreicherung begünstigen. Diese Stoffe sind z.B. bei GMO für den Knoblauchgeruch verantwortlich. Es gibt allerdings viele verschiedene und man kann sie den Gas/Knoblauch Noten am meisten zuordnen, wenn man nicht zwischen den einzelnen unterscheidet. Eines der besten Paper zu diesem Thema ist (Oswald et al. 2021).
Abbildung 10: VSC Analyse von Bacio Gelato (Oswald et al. 2021)
Kohlenstoff
Keiner der klassisch gewerteten Pflanzennährstoffe, jedoch essenziell ist der Kohlenstoff. Dieser wird über die Luft aufgenommen als CO2 und fungiert als Quelle des Kohlenstoffs für die Glucoseherstellung (Zucker) bei der Photosynthese. Er hat aber auch noch weitere wichtige Aufgaben im Boden. Zunächst ist jeder organische Stoff und viele wichtige Chelatierungsmittel (verfügbarkeitssteigernd), wie Huminsäure, Kohlenstoff basiert. Sie dienen als Trägermittel für die meisten Nährstoffe und sind der Grundstein allen Leben.
Die Speicherung des atmosphärischen CO2s aus der Luft in der Pflanze und im Boden nach dem Schnitt, ist der Schlüssel zur Reduktion von Treibhausgasen in der Atmosphäre.
Dieser Prozess wird CO2 Sequestrierung genannt und durch sorgfältige Rechnung und Ausgleichsflächen kann somit ein Ausgleich für die entstandenen Emissionen (Dünger/Traktor/Verarbeitung) geschaffen werden. Dies ist die Grundlage der nachhaltigen Landwirtschaft und die einzige Möglichkeit bisher wirklich effizient klimawirksame Gase aus der Luft zu entfernen.
Zudem wird dies in Zukunft eine wertvolle Marktgrundlage für den Emissionshandel. Berechnet wird das ganze mit einem Kohlenstoffsaldo und es werden Zusatzpunkte/Abzüge für bestimmte Methoden vergeben. Ein gutes Review zur Methodik wurde durch Prof. Dr. Hülsbergen mit veröffentlicht, von welchem ich auch über dieses Thema gelernt habe. (Küstermann et al., 2008)
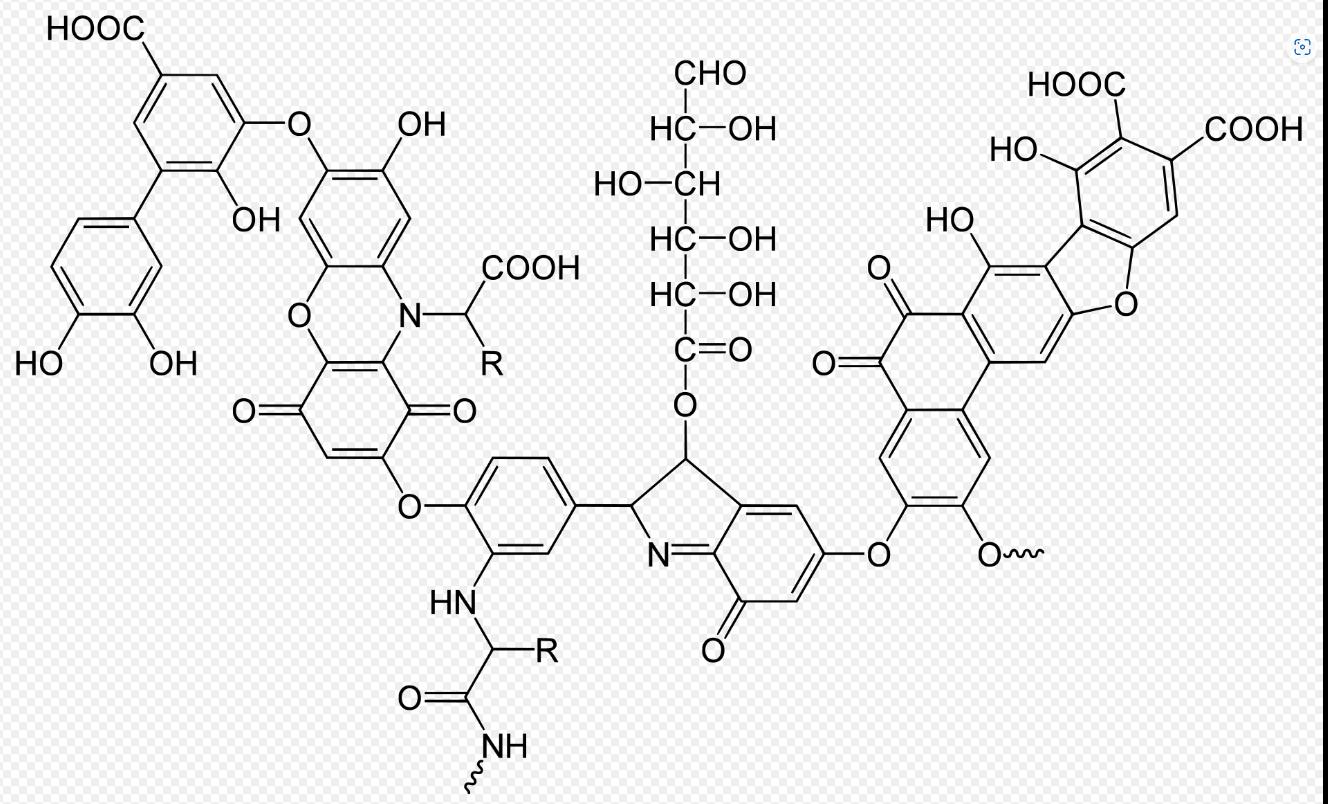
Abbildung 11: Formel Huminsäure (Stevenson 1994)
Mikronährstoffe
Alles unter 100 g/kg Pflanzenmasse trocken wird als Mikronährstoff bezeichnet, diese sind Eisen, Bor, Molybdän, Kupfer, Zink und Chlor. Besonders Molybdän, Bor und Eisen sind häufige Mangelerscheinung bei Cannabis also sollte hier besonderes Augenmerk darauf gelegt werden (Cockson et al. 2019a). Die meisten Mikronährstoffeffekte beziehen sich auf die Verwendung als Co-faktor in Enzymen oder sind in der Elektronentransportkette des Mitochondriums beteiligt.
Bor nimmt
Abbildung 12: Kupferabhängige Enzyme (Pandey 2018)

Abbildung 13: Manganabhängige Enzyme (Pandey 2018)
Abbildung 14: Molybdän abhängige Enzyme (Pandey 2018)
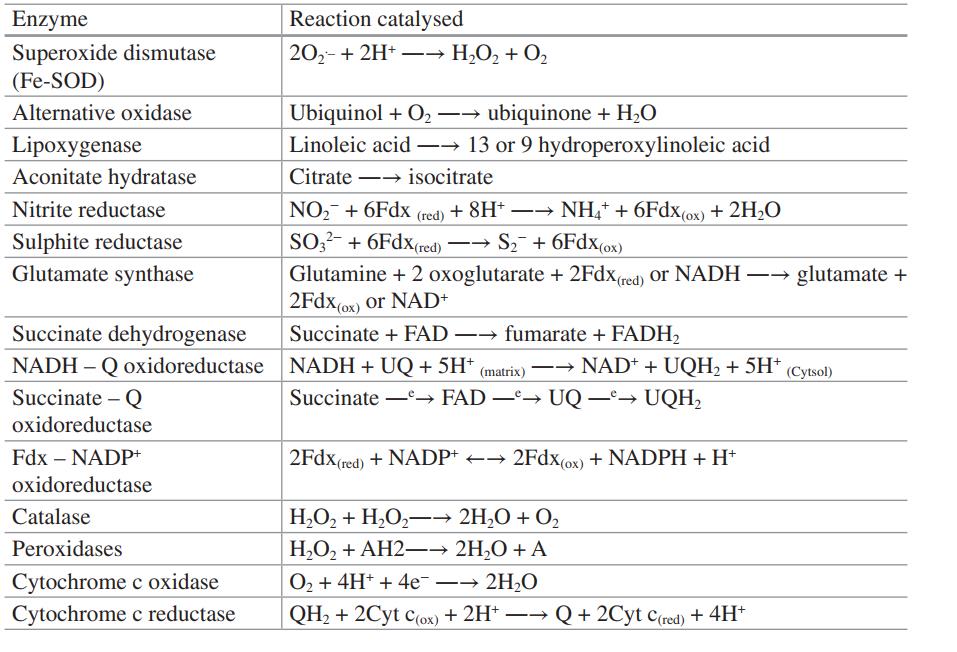 Abbildung 15: Verschiedene Eisen-abhängige Enzyme (Pandey 2018)
Abbildung 15: Verschiedene Eisen-abhängige Enzyme (Pandey 2018)
Zusatzstoffe / Stärkungstoffe
Silikon
Damit Pflanzen ihre strukturelle Integrität bewahren können, benötigen sie den Mikronährstoff Silizium. Er trägt zur Bildung von Zellwänden und zur Steuerung des Pflanzenwachstums bei. Zusammen mit Kalzium verleiht dieser Nährstoff den Pflanzen ihre eigentliche Stärke. Er ist von entscheidender Bedeutung, da die Knospenfäule leicht in die großen Knospen eindringen und sich dort entwickeln kann, vor allem unter Bedingungen mit hoher Intensität (1000umol/m2*s, 1200ppm CO2, usw.). Darüber hinaus verringert es den Bedarf an Bindearbeiten und hilft, sehr schwere Äste zu stärken, die sonst brechen könnten. Dies ist besonders wichtig für den ursprünglichen GG #4-Schnitt, der von Natur aus große Blütenstände bildet und überall hinfliegt. In Bezug auf Cannabis haben einige Studien gezeigt, dass bestimmte Mikronährstoffe spezifische Funktionen in Cannabispflanzen haben können. Eine Studie, die im Journal of Plant Nutrition and Soil Science veröffentlicht wurde, ergab beispielsweise, dass Zinkmangel in Cannabispflanzen zu vermindertem Wachstum und verminderter Cannabinoidproduktion führen kann (Landi 1997).
Es gibt noch weitere Stoffe, die die Pflanzenernährung beeinflussen, aber nicht direkt als Nährstoff aufgenommen werden. Sie haben teilweise positive, aber auch negative Effekte.
Natrium
Dieses Element ist in den meisten Nährstoffträgern wie Kelp oder Muschelschalen, welche aus dem Meer stammen enthalten. Es wird nicht von der Pflanze direkt benötigt und eine Akkumulation ist sogar schädlich für die Pflanze, da der Stoff die anderen Nährkationen verdrängt mit seiner positiven Ladung. Deshalb sollte bei jedem Zusatzmittel des Bodens darauf geachtet werden, eine möglichst geringe Menge an Natrium einzutragen. Dies ist eine der häufigsten Ursachen, zusammen Bicarbonat Anreicherungen, für Nährstoff Dysbalancen in MGMs.
Chlor
Die Aufrechterhaltung des Turgors und der Osmoregulation ist eine wesentliche Funktion von Chlor in Pflanzen. Zu den osmoregulatorischen Funktionen von Chlor gehört seine Beteiligung an der turgorgesteuerten Zellentwicklung und der Funktion der Stomata. Chlor reichert sich in großen Mengen in den Wurzel- und Sprossspitzen an, wo es an der turgorbedingten Entwicklung der Zellfortsätze beteiligt ist. Dennoch sollten zu hohe Werte vermieden werden, um die oxidierende Wirkung auf Bakterien und das Mikroleben einzuschränken.
Meist wird genug Chlor über Komposte oder das Wasser ins System eingetragen, um es nicht extra supplementieren zu müssen.
Umrechnungsformeln und chemische Nährstoffformen
Es muss beachtet werden, dass in den Amendments die Gehalte meist in ihrer gebunden Form wie z.B. P2O5.
Der Umrechnungsfaktor zwischen P2O5 und P hängt vom Molekulargewicht der jeweiligen Verbindung ab.
Das Molekulargewicht von P2O5 beträgt 141,94 g/mol, und es enthält zwei Phosphoratome.
Das Molekulargewicht von P beträgt 30,97 g/mol.
Um P2O5 in P umzurechnen, muss man den P2O5-Wert mit 0,4364 multiplizieren (oder durch 2,29 dividieren).
Das bedeutet, dass 1 Gramm P2O5 0,4364 Gramm P enthält.
Um von P2O5 in P umzurechnen, können Sie daher folgende Formel verwenden:
P = (P2O5 * 0,4364)
Oder
P2O5 = (P / 0,4364)
Hier ist eine Liste aller pflanzenverfügbaren Formen von Nährstoffen, die Reinstoffmenge könnt ihr euch wie im Beispiel oben errechnen
- Stickstoff (N)
- Nitrat (NO3-)
- Ammonium (NH4+)
- Phosphor (P)
- Orthophosphat (H2PO4- and HPO42-)
- Mono- und Diester der Phosphorsäure (organisches P)
- Potassium (K)
- Kalium-Ionen (K+)
- Calcium (Ca)
- Calcium-Ionen (Ca2+)
- Magnesium (Mg)
- Magnesium-Ionen (Mg2+)
- Sulfur (S)
- Sulfat (SO42-)
- Elementarer Schwefel (S) in oxidierten Böden
- Eisen (Fe)
- Eisen (Fe2+)
- Mangan (Mn)
- Mangan-Ionen (Mn2+)
- Zink (Zn)
- Zink-Ionen (Zn2+)
- Kupfer (Cu)
- Kupfer-Ionen (Cu2+)
- Bor (B)
- Borax (Na2[B4O5(OH)4])
- Chlor (Cl)
- Chlorid (Cl-)
- Molybdän (Mo)
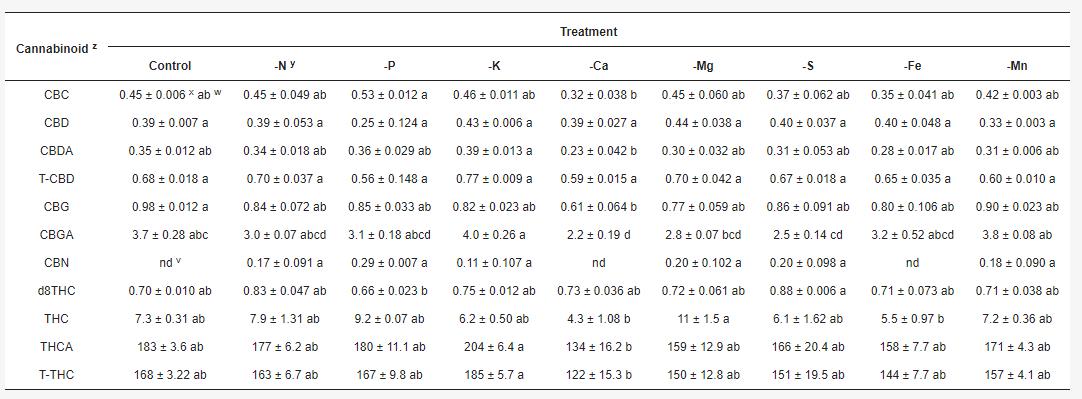
Mängel dieser Elemente führen zu Einbußen in der generellen Biomasse und zur Abnahme der Ernteindexes. Um die Auswirkung zu quantifizieren haben (Llewellyn et al. 2023) eine sehr umfangreiche Studie angelegt, welche die Auswirkungen gemessen hat.
Abbildung 16: Frischgewicht (FW) des abgetrennten oberirdischen Gewebes, Ernteindex (Blütenstand FW/Stängel und Blätter FW) und Trockengewicht (DW) der Wurzeln aus jeder Nährstoffbehandlung. (Llewellyn et al. 2023)
Abbildung 17: Veränderung der Cannabinoidzusammensetzung unter bestimmten Nährstoffmängeln (Llewellyn et al. 2023)
Diese Einbußen sind jedoch spezifisch für den Ort des Organs, da Pflanzennährstoffe entweder mobil oder immobil in der Pflanze selbst sind.
Das Konzept der mobilen und immobilen Nährstoffe bezieht sich darauf, wie leicht sich diese Nährstoffe innerhalb einer Pflanze bewegen können, nachdem sie von den Wurzeln aufgenommen wurden. Mobile Nährstoffe können leicht von älteren zu jüngeren Pflanzengeweben wandern, während unbewegliche Nährstoffe in den Geweben verbleiben, in denen sie ursprünglich aufgenommen wurden.
Zu den mobilen Nährstoffen gehören Stickstoff (N), Phosphor (P) und Kalium (K), die für das Pflanzenwachstum wichtige Makronährstoffe sind. Diese Nährstoffe können innerhalb der Pflanze leicht über das Phloem transportiert werden, ein spezialisiertes Gefäßgewebe, das Nährstoffe und Zucker durch die Pflanze transportiert.
Zu den immobilen Nährstoffen gehören dagegen Kalzium (Ca), Schwefel (S) und viele Mikronährstoffe wie Eisen (Fe) und Zink (Zn). Diese Nährstoffe lassen sich nicht so leicht innerhalb der Pflanze transportieren und verbleiben in den Geweben, in denen sie ursprünglich aufgenommen wurden.
Die Mobilität der Nährstoffe kann wichtige Auswirkungen auf das Wachstum und die Entwicklung der Pflanzen haben. Wenn eine Pflanze beispielsweise einen Mangel an einem mobilen Nährstoff wie Stickstoff hat, wird sie Stickstoff von älteren Blättern auf jüngere Blätter übertragen, um das Wachstum aufrechtzuerhalten. Dies kann dazu führen, dass ältere Blätter gelb oder braun werden, da sie keinen Stickstoff mehr enthalten.
Im Gegensatz dazu kann ein Mangel an einem immobilen Nährstoff wie Kalzium zu einem verkümmerten Wachstum oder zu Missbildungen in den betroffenen Geweben führen, da der Nährstoff nicht ohne weiteres in andere Teile der Pflanze transportiert werden kann, um das Wachstum zu unterstützen.
Dies ist immens wichtig, um Mängel frühzeitig eingrenzen zu können und entsprechende Nachdüngung zu veranlassen. Eines der besten Paper auf dem Gebiet und eins der ersten bei medizinischen/aktuellen Kultivaren ist das von (Cockson et al. 2019b).
Der PH-Wert und der Einfluss auf die ionische Form der Nährstoffe
Um ein maximales Wachstum und eine optimale Entwicklung zu gewährleisten, muss sichergestellt werden, dass die Cannabispflanzen die richtige Mischung aus jedem dieser 16 Nährstoffe erhalten. Cannabispflanzen haben je nach ihrem Entwicklungsstadium, der Art und dem pH-Wert ihres Bodens und dem Vorhandensein anderer Nährstoffe einen unterschiedlichen Nährstoffbedarf. Um den Nährstoffgehalt ihres Bodens zu ermitteln und ihre Düngeverfahren entsprechend anzupassen, können die Anbauer Bodentests und die Analyse von Pflanzengewebe einsetzen, denn die Ladung und Form der Nährstoff wird durch das Milleu beeinflusst.
Meist liegen die oben genannten Nährstoffe nämlich nicht in neutraler Form vor bzw. sind selbst schon Ionen. Die Ladungen spielen eine wichtige Rolle in der Aufnahme von Nährstoffen durch die Wurzeln. Bisher wurde die Aufnahmefähigkeit von Nährstoff anhand der Tabelle von (Peterson 1982) genutzt.

Abbildung 18: Verfügbarkeit Nährstoffe in einem torfbasierten und angereichertem System (Peterson 1982)
Neuste Studien von (Hartemink und Barrow 2023) zeigen allerdings, dass dies nicht so einfach anwendbar ist. Es spielen noch so viele Interaktionen wie z.B. die verschiedenen Auswirkungen von Mikroben Gemeinschaftsveränderungen durch Exudate eine Rolle, dass man diese PH-Ranges nur für inerte Systeme schätzend verwenden kann. Selbst dies ist noch ungenau, es müssten zudem noch Einflüsse der Wurzelausscheidungen auf den PH und die Mineralisierungsraten bestimmt werden, um akkurate Aussagen treffen zu können. Dies aber sprengt schon wieder den Rahmen des Möglichen im Heimanbau. D.h. insbesondere in living soil System kann weder der PH-Wert des Wassers noch der des Bodens akkurate Aussagen über Nährstoffe geben. (Hartemink und Barrow 2023).
Grob ist dies trotzdem zu beachten im Anbau. Denn ein Boden PH von z.B. > 9, leidet ziemlich sicher an einer zu hohen Ansammlung von Calciumcarbonat oder ähnlichen Stoffen. Hier wird die Aufnahme von Nährstoffen stark eingeschränkt, insbesondere die der Mikronährstoffe, welche für die Regulation fast aller Prozesse und für die Enzyme essenziell sind. Für die reine mineralische Verfügbarkeit von Nährstoffen sind 5.5-5.8 optimal so wie er auch im mineralisch, kommerziellen Anbau genutzt wird.
Ein pH-Wert unter 6.0 wird dann aber wieder problematisch für das Mikrobiom, da dieses unter 6.0 teilweise in ein anaerobes, heterofermentatives Milleu wechselt, welches wir zwar in bestimmten Phasen (Stretch/Flower I), aber in den meisten Phasen nicht wollen. Hier wollen wir einen pH von 6.0-6.8 halten, da hier die meisten nützlichen Mikroorganismen leben, siehe 2.3.1 Mikro Flora.
Wenn man nun ein optimales, Kultivar spezifisches Rezept erstellen möchte, kann man je nach Nährstoffbedarf des Kultivars den p.H. weiter oben oder unten ansetzen. Mein persönlicher Sweet spot ist bei 6.5 in der Vegetativen Phase, welcher sich dann auf 6.3 im Verlauf der Blüte senkt. Dies ist wie oben aber erwähnt auch nur ein Schätzwert, da das mikrobielle Leben mit eingerechnet werden muss. Im nächsten Kapitel sehen wir nämlich auch, dass die Pflanzen/Mikrobeninteraktion über die Ausschüttung von Zuckern und die subsequente Vermehrung spezieller Mikroben durch die Pflanze einen erheblichen Einfluss hat. Damit steuert also die Pflanze die meisten Vorgänge und wir geben ihr mehr oder weniger nur die Werkzeuge, um sich selbstständig, optimal entfalten zu können.
Die Aufnahme der Nährstoffe an den Wurzeln
Pflanzen nehmen Nährstoffe über ihre Wurzeln in Form von Ionen auf. Diese Ionen gelangen über 3 Mechanismen an der Wurzel. Diese sind Interzeption, Massenstrom und Mikrobielle Interaktion, wobei der Erste sich auf das Hindurchwachsen der Wurzeln und die subsequente Aufnahme beziehen. Der Zweite Mechanismus (Massenstrom/Massenfluss) bezeichnet den Transport mittels Wassers, welches direkt Ionen in die Wurzel einspült, dies kann auch von Nachteil sein, wenn in der Nährlösung des Bodens eine zu hohe gelöste Ionenkonzentration (zu hoher EC-Wert) erreicht wird. Dann kann sich die Pflanze sozusagen nicht mehr gegen den Nährstoff wehren und wird überdüngt / zwangsernährt. Dies hat leider nicht wie bei der Gänsestopfleber zur Folge, dass das Endprodukt besser schmeckt, sondern eher das Gegenteil und es „verbrennt“ die Pflanze. Darum müssen wir bei Tests (Kapitel 3. Wie teste ich dies Bestandteile meines Bodensystems) immer auf die Mineralisationsrate achten, diese stellt man fest, indem man Vorratstests (Merlich III) mit Lösungstests (saturated paste) vergleicht und die % Lösung/Zeiteinheit misst. Dies ist natürlich nur ein Schätzwert, da wir keine Real time data zur Mineralsationsrate haben. Ist diese zu hoch, wird auch der EC-Wert unserer Bodenlösung zu hoch und die Pflanzen gehen ein.
Der dritte Weg wie Nährstoffe in die Pflanzen kommen ist die Interaktion von Mikroben (meist arbuskuläre Endomykhorizza) mit den Wurzeln. Genaue Mechanismen und präferierte Nährstoffe für diesen Aufnahmemechanismus werden im Kapitel 2.3.2.2 Pilze (PGPFs) behandelt.
Die Bewegung der Ionen in und aus den Pflanzenzellen bei der Interzeption wird durch das Konzentrationsgefälle geregelt, d. h. den Unterschied in der Ionenkonzentration zwischen dem Inneren und dem Äußeren der Zelle. Wenn die Ionenkonzentration an der Außenseite der Zelle höher ist als an der Innenseite, strömen Ionen in die Zelle, um die Konzentration auszugleichen. Diese Bewegung von Ionen in die Zelle und aus der Zelle heraus wird durch Ionentransporter erleichtert, bei denen es sich um Proteine handelt, die dabei helfen, Ionen durch die Zellmembran zu bewegen. (Wang et al. 2006)
Zudem werden höher geladene Stoffe wie Mg2+ stärker aufgenommen als K+ mit einer Ladung. Dies kann bei zu hoher Konzentration einzelner Stoffe zu einem Verdrängungseffekt an der Wurzel führen, da nur die stark geladenen Mg2+ aufgenommen werden, aber die schwachen K+ erstens nicht durchkommen und zweitens von dem Mg2+ abgestoßen werden, da sie die gleiche Ladung besitzen. Dies zeigt die immense Wichtigkeit der Balance im System, MGMs sind wie Ballet und nicht wie ein Strongman Wettbewerb, es zählt Harmonie und nicht viel hilft viel. Inbesondere die Kationen müssen im Auge behalten werden, denn zwar können die Mikroben viel ausgleichen, aber eben auch nicht alles. Wir schaffen, wie vorher angesprochen, den perfekten Werkzeugkasten für die Pflanze und wenn zu viele Nägel da sind, findet die Pflanze keine Schrauben mehr, um es etwas anschaulicher zu formulieren. Mehr dazu im Kapitel 2.2.4 CEC und AEC – Kationen und Anionen Austausch Kapazität und Basissättigung
Und hier nochmal ein Schema zur Nährstoffaufnahme anhand eines Wurzelquerschnitts
Abbildung 19: Schema zur Nährstoffaufnahme anhand eines Wurzelquerschnitts (Wang et al. 2006)
Wir sehen hier auf der linken Seite den passiven Transport. Dieser ist vorallem für Stickstoffderviate und andere geladene Nährstoffe gedacht. Die Pflanze muss hier keine „Arbeit“ verrichten, da es entlang des natürlichen H+ Gradienten einströmt. D.h. die Ladung innerhalb der Wurzel passt so, dass die Nährstoffe aufgenommen werden können und die Anionen/Kationen Balance trotzdem noch passt.
Aktiver Transport wird genutzt, wenn der arbeitsfreie Aufnahmeweg blockiert ist. Es wird hierbei entweder H+ aus der Wurzel ausgestoßen bei Kationenaufnahme, da sonst zu viel + Ladung in der Wurzel ist. Diese Kanäle werden als Antiporter bezeichnet.
Bei Anionen Aufnahme entgegen des natürlichen Gradientens, wird ein Symporter Kanal genutzt. Dieser packt das – geladene Teilchen zusammen mit einem H+ Atom, um auch hier wieder die Balance zu halten und das Ladungsgleichgewicht nicht zu stören. Zusammenfassend kann man sagen, die Pflanze muss immer ein Ladungsgleichgewicht halten und tauscht mit dem Boden entweder gleiche oder verschiedene Ladungen aus. Die Pflanze kann die innere Ladungszusammensetzung auch steuern, aber präferiert es natürlich immer möglichst wenig Arbeit selbst zu verrichten.
Aus diesem Grund gibt auch höhermolekulare, organische Verbindungen wie Aminosäuren, die aufgenommen werden können und der Pflanze somit weniger Aufbauenergie (ATP) kosten als niedermolekulares Nitrat, kosten. Diese müssen allerdings direkt über das Blatt appliziert werden, denn im Boden werden sie durch die Mikroben vorverdaut und sind dann wieder reines Nitrat, welches, dann erst wieder aufgebaut werden muss. D.h. Aminosäurendüngung über den Boden ist relativ nutzlos für die Pflanze selbst, allerdings kann man es als Nahrung für Mikroben nutzen, da würde ich allerdings keine teuren reinen Aminos nehmen, sondern Kompost oder frischen Grünschnitt. Hier nochmal ein Überblick über den Stickstoffzyklus der Pflanze, welcher mit Glutamin aus Nitrat beginnt und somit die Basis für sämtliche Aminosäuren dieses Planeten bildet. Es gibt fast keine anderen Organismen, welche diesen Schritt können. Ohne sie, würde es auch keine Menschen oder Tiere aus Fleisch geben (Tegeder und Rentsch 2010). Welche Transporter für welche Funktion zuständig sind, sehen wir in Abbildung 10&11.
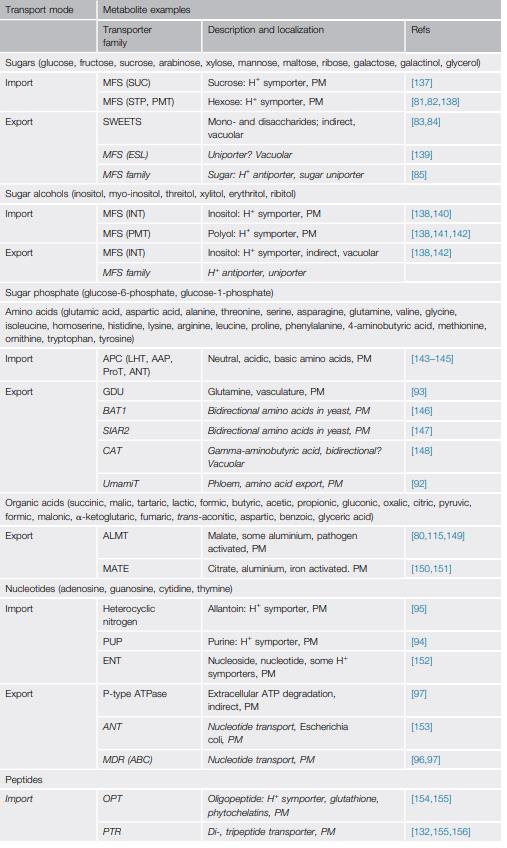
Abbildung 20: Transporter Modus operandi pt1 (Sasse et al. 2018)
Abbildung 21: Transporter Modus operandi pt 2 (Sasse et al. 2018)
Wir haben uns bereits die Aufnahme der Pflanzennährstoffe auf chemischer Ebene angeschaut, jetzt fehlt aber noch die angesprochene Interaktion von Pflanze und Mikroben. Die Pflanzen können nämlich bestimmte Polysaccharide / Monosaccharide (mehrfach/einfache Zucker) aus ihren Wurzeln ausscheiden, welche dann als spezifische Nahrung für spezifizierte Mikroben dient. D.h. die Pflanze kann selbstständig, wenn sie alle nötigen Stoffe besitzt/gesund ist, die Zusammensetzung des Mikrobioms steuern.
Benötigt die Pflanze nun mehr Phosphor z.B. werden Zucker mittels der SWEETS oder MFS-Transporter in die Rhizosphäre exportiert, wie man in Abbildung 10 sehen kann. Darüber hinaus produzierten Arabidopsis-Pflanzen (Modell Organismus) mit Phosphatmangel mehr Cumarin und Oligolignol, mit Schwermetallen behandelte Pappeln (Populus tremula) mehr organische Säure und Weizen mit Zinkmangel mehr Phytosiderophore. Die unterschiedliche Exsudation ist ein möglicher Weg, auf dem Pflanzen ihre Interaktionen mit Mikroorganismen verändern können, wie der Zusammenhang zwischen Exsudationsmustern und Rhizobiomvariationen bei acht Arabidopsis-Linien zeigt. Damit und mit den Abbildungen 10&11 sehen wir, dass Pflanzen nicht nur diese Zucker zur Mikrobeninteraktion exsudieren sondern auch organische Säuren (Ausspaltung Nährstoffe & pH Regulation), Aminosäuren und weitere Chemikalien ausstoßen können. Dies hat hunderte regulatorische Effekte. Das beste systematische Review zu dem Thema findet ihr bei (Sasse et al. 2018)
Genauere Informationen zu den Organismen werden im Kapitel 2.3.1 Mikro Flora behandelt.
Es werden bis zu 20% der gesamten hergestellten Zucker der Pflanze (Photosynthese / Calvin Zyklus) für diese Interaktionen aufgewandt, wenn es benötigt wird. (Sasse et al. 2018) Diese Zahl gilt es so zu vermindern, dass wir mit mineralischen Nährstoffen, welche keine mikrobielle Aufspaltung benötigen, den Grundbedarf decken und die spezifischen Eigenheiten der Kultivare durch die Mikroben decken lassen. D.h. auch hier ist eine Balance wieder von höchster Wichtigkeit. Wir wollen nicht alles von den Mikroben herstellen lassen, sondern nur die Feinjustierung der Nährstoffe. Der Grundbedarf wird durch Mineralien/mineralisierte Nährstoffe bereitgestellt. Dies ist auch der Grund für die optimale Ausprägung des
2.2.5 CEC und AEC – Kationen und Anionen Austausch Kapazität und Basissättigung
Nun haben wir sowohl den Bodenwasservorrat angeschaut als auch welche Nährstoffe sich in diesem Wasser lösen können. Jetzt benötigen wir nur noch Informationen über die Nährstoffspeicherfähigkeit unseres Bodens.
Die Kationenaustauschkapazität (CEC) beschreibt die Fähigkeit eines Materials, positive Ladungsträger (Kationen) auszutauschen. Das Gegenstück dazu ist die Anionenaustauschkapazität (AEC), die die Fähigkeit eines Materials beschreibt, negative Ladungsträger (Anionen) auszutauschen.
Die CEC und AEC von Torf werden in der Regel in Milliequivalenten pro Gramm (meq/g) gemessen. Die CEC und AEC von Torf hängen von verschiedenen Faktoren ab, wie zum Beispiel der chemischen Zusammensetzung des Torfs, der Größe und Form der Torfpartikel und den Bedingungen, unter denen der Austausch stattfindet.
Anders als im gewachsenen Boden aus Sand, Schluff und Ton, ist unser Torfbasiertes System ohne Zusätze noch ziemlich karg, was die Speicherfähigkeit für Pflanzennährstoffe anbelangt. Im normalen Boden gibt es hierfür Ton- und andere Mineral Verbindungen mit positiv/negativ geladener Oberfläche.
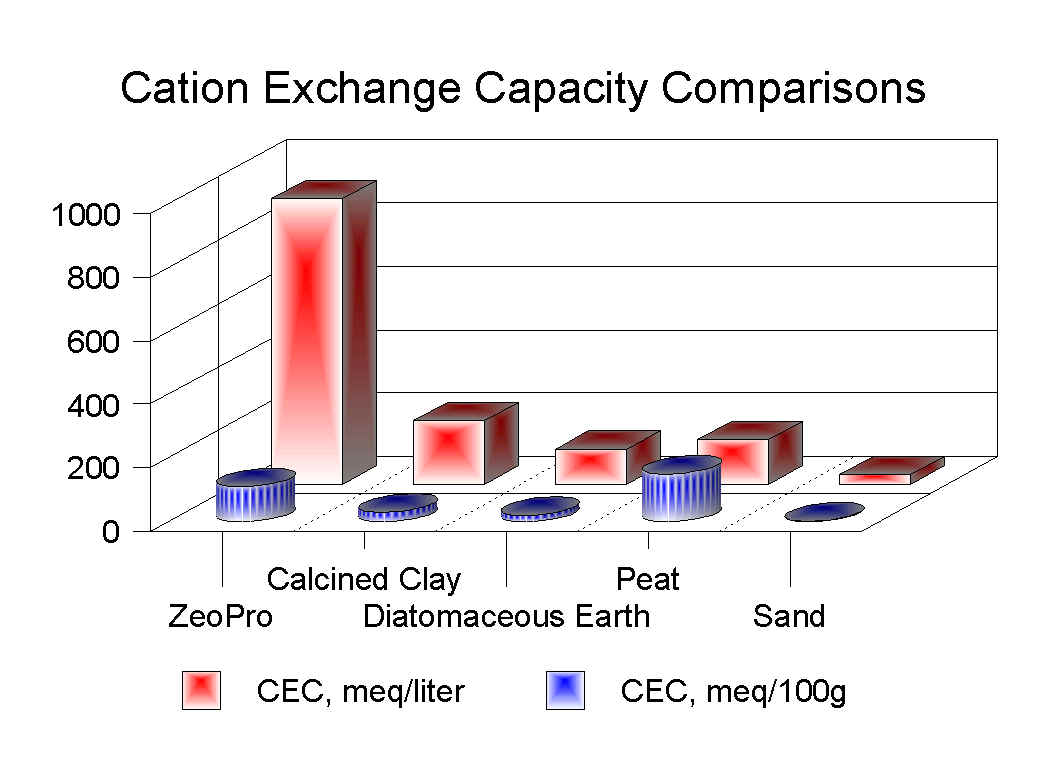
Abbildung 22: Kationenaustauschkapazität verschiedener Materialien (Andrews 2013)
Torf enthält viele Quarzsandkörner und organische Bestandteile, die beide elektrisch geladen sind. Die organischen Bestandteile haben eine negative Ladung, während die Quarzsandkörner eine positive Ladung haben. Wenn Torf in Kontakt mit Wasser kommt, können die Kationen und Anionen aus der Lösung an die elektrisch geladenen Teilchen im Torf binden. Dieser Austauschprozess wird als Adsorption bezeichnet.
Bodenzusätze wie Mineralien (Zeolit, Langbeinite usw) als auch organische Stoffe wie Humus/Kompost verbessern die Speicherfähigkeit des Bodens und werden deshalb zugesetzt. Sie tragen also nicht nur zur Füllung an sich also den reinen Nährstoffen bei, sondern auch zur gesamten Speicherfähigkeit des Bodens.
Der Prozentsatz der Füllung von CEC/AEC wird als Basensättigung bezeichnet und ist von den jeweiligen Kationen/Anionen, die bereits in 2.2.1 erwähnt wurden und vom PH Milleu abhängig. (Blume et al. 2010)
Es gibt keinen "optimalen" Wert für die Kationenaustauschkapazität (CEC) von Torf in Cannabis-Anbau-Systemen, da die ideale CEC von vielen Faktoren abhängt, einschließlich der Art der Cannabispflanze, der Nährstoffanforderungen der Pflanze und den Bedingungen des Anbaus. In der Regel wird eine höhere CEC als vorteilhaft betrachtet, da sie dazu beitragen kann, dass mehr Nährstoffe von den Pflanzen aufgenommen werden. Allerdings kann eine zu hohe CEC auch dazu führen, dass zu viele Nährstoffe in der Pflanze gebunden werden, was zu einem Nährstoffmangel führen kann
Gemessen wird er in meq/100g (milliequivalenten/100g). Die einzelnen Stoffe und ihre CEC findet ihr Kapitel 2.4. Diese Milliequivalente lassen sich in mg/kg umrechnen mit dem jeweiligen Umrechnungsfaktor der spezifischen Elemente:
Tabelle 2: CEC Umrechnungsfaktoren (Local Land Services (NSW Government) 2020)
| Kation | mg/kg oder ppm(A) | Umrechnungsfaktor (B) | meq/100g (A/B) |
| Ca2+ | 582 | 200 | 2,91 |
| Mg2+ | 168 | 122 | 1,38 |
| K+ | 59 | 390 | 0,15 |
| Na+ | 27 | 230 | 0,12 |
Um den vollständigen CEC zu berechnen, müssen noch die meq/100g von Aluminium und dem freien Wasserstoff miteingefügt werden. Allerdings wird meistens auf die vier Hauptkomponenten geachtet, da freier Wasserstoff in geringen Mengen auftritt (bei angemessenem pH von 6.2-6.8) und in einem gesunden Boden das Aluminium so oder so nicht in hoher Menge vorhanden sein soll. (Local Land Services (NSW Government) 2020)
Der CEC lässt sich mit den Hauptkationen in Tabelle 1 in verschiedenen Verhältnissen füllen. Die optimalen Werte die heutzutage verwendet werden basieren hauptsächlich auf den Werken von (ALBRECHT 1959). Verschiedene Kulturen und verschiedene Setups müssen natürlich immer leicht nach Gegebenheiten angepasst werden. So brauchen z.B. schwere Böden mehr Calcium als Magnesium im Verhältnis zu leichteren Böden. Dies liegt an der gröberen Struktur des Calciums und den daraus resultierenden zusätzlichen Poren.
Es werden drei Referenzwerte, einmal von (Logan Labs 2023), einmal von (ALBRECHT 1959) und einmal von AgPHD auf Youtube, welche ich auch nur jedem empfehlen kann, verglichen.
Tabelle 3: Vergleich verschiedener Baissättigungsreferenzwerte
| Kation/Method | Albrecht | Logan Labs | AgPHD |
| Ca2+ | 68-70% | 60-70% | 65-80% |
| Mg2+ | 10-12% | 10-20% | 12-20% |
| K+ | 4% | 2-5% | 4-8% |
| Na+ | So niedrig wie möglich | So niedrig wie möglich | So niedrig wie möglich |
Um nun die optimalen Werte in PPM Nährstoff umzurechnen, benutzt man die Formel
CEC x Nährstoffspezifischer Wert x gewählte % Basissättigung
25 (CEC für Beispielboden) x 400 (Wert für Calcium) x 70% (Albrecht %satz für Calcium)
= 7000kg/ha = 0.7 kg/m² = 700g/m2 Calcium pro m2 Beet
7000kg/ha / 2.24 = 3125mg/kg Boden (Local Land Services (NSW Government) 2020) l
=> optimaler Wert
Ein Beispiel wie man nun auf die benötigte Aufdüngemenge mit einem echten Bodentest kommt, findet man im Kapitel 3.2.5 Kationen und die Basissättigung
Der errechnete Wert ist leider in kg/ha also schwierig auf Indoorbeete anzupassen. Man kann allerdings grob rechnen und den A Horizont mit 0,5m schätzen und somit dann die ha auf m2 Beet runterrechnen.
Die Nährstoffspezifischen Werte der Kationen sind:
Calcium: 400
Magnesium: 240
Kalium: 780 (Logan Labs 2023)
Biologische Faktoren / Das Soil food Web
Als "Soil Food Web" wird meist in den gängigen Foren das komplexe Ökosystem im Boden beschrieben, welches aus unterschiedlichen Arten von Mikroorganismen, Pilzen, Würmern, Insekten und anderen Tieren besteht. Dieser Begriff wurde durch Dr. Elaine Ingham bekannt gemacht und verbreitet, wobei die aktuelle Wissenschaft sich auch dreht und dem Soil food web immer mehr Bedeutung zu misst.
Die Lebewesen interagieren miteinander und bilden ein dynamisches Netzwerk von Beziehungen, in dem Nährstoffe und Energie auf vielfältige Weise umgeleitet werden. Das Soil Food Web wird als die Lebendigkeit des Bodens betrachtet und ist wichtig für die Gesundheit des Bodens, und durch den Boden beeinflusst die Nährstoffversorgung, Widerstandsfähigkeit gegen Schädlinge, Wasseraufnahme und die Möglichkeit von Pflanzenwachstum.
Der Kreislaufaspekt wird für uns umso nützlicher, da Genera wie Bakterien von größeren Wesen wie den Protozoa oder Würmern gefressen und verdaut werden, was dann bei der Ausscheidung die Nährstoffe mineralisiert für die Pflanze bereitstellt. Bei der Verdauung durch Würmer werden sogar noch durch Huminsäuren zusätzliche Nährstoffe chelatisiert. Dieser Zyklus geht über alle Stufen bis es schlussendlich Makrowesen wie Vögel inkludiert, welche wir im indoor Anbau leider nichtn haben, diese werden aber durch das Umgraben / mechanische Töten des Bodens/seiner Lebewesen simuliert also ist es schon fast ein kompletter Zyklus.
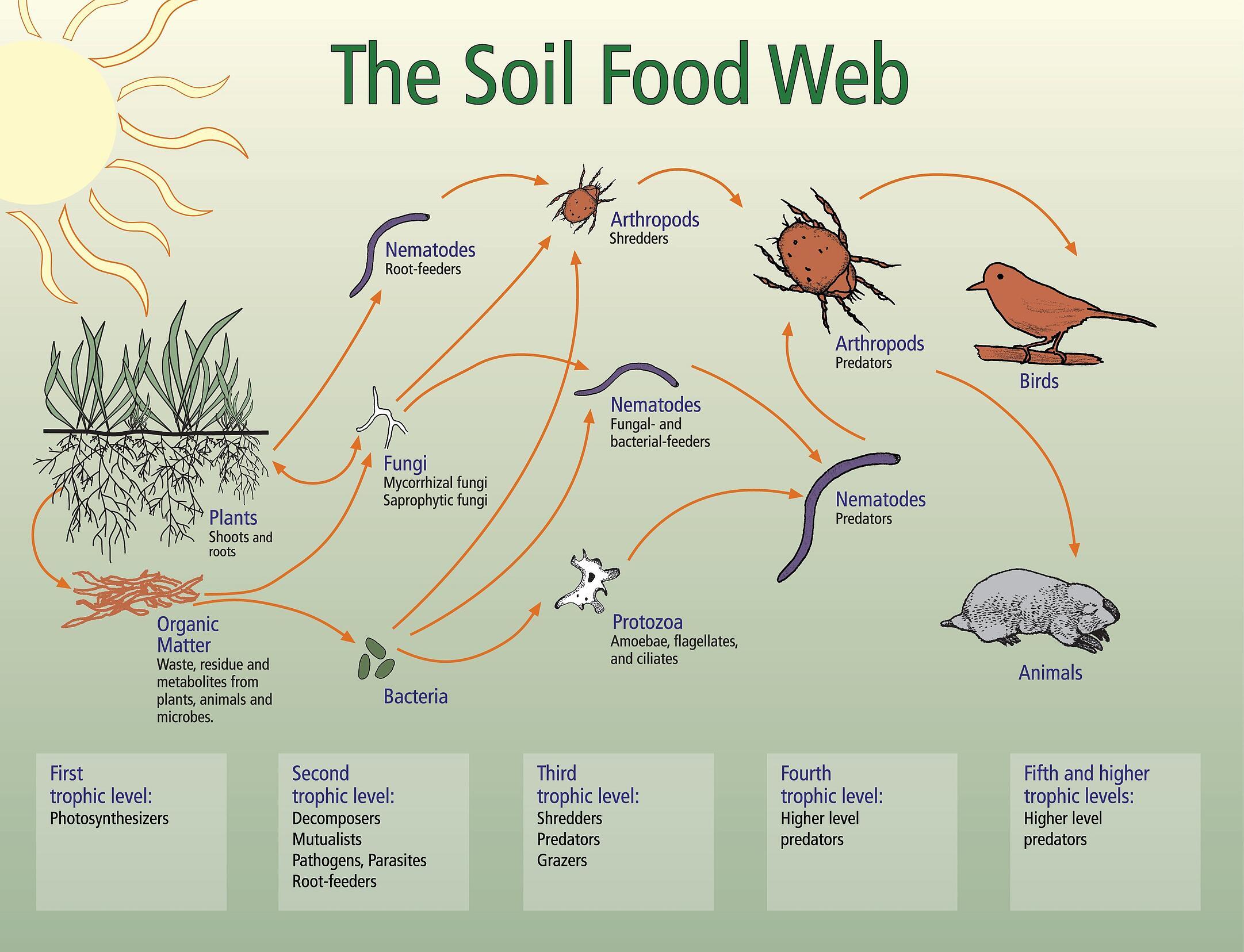
Abbildung 23: Das Soil Food Web - Schema (Natural Resources Conservation Service 2023)
Wir schauen uns jetzt einzelnen Teile genau an und klären welchen Nutzen sie im Gartenbaubereich haben.
Einteilen können wir diese Lebewesen weiter in Mikro Fauna und Mikro Flora, wobei Fauna die aktuell vorliegende Tierdiversität und Flora die aktuell vorliegende Pflanzendiversität darstellt.
Mikro Flora
Bakterien
Dieser kleinste Teilnehmer der Mikrofauna ist das Bakterium. Es gibt enorm viele Strains von ihnen (dies ist die korrekte Verwendung von Strain, Cannabis hat varieties) und viele besitzen für das Pflanzenwachstum positive Eigenschaften. Diese Gruppe fasst man als PGPR (Plant growth promoting) Bakterien zusammen.
Diese haben direkte und indirekte Auswirkungen auf die Pflanze, hier eine Liste der Prozesse, die sie begünstigen. Wen es genauer interessiert kann einen groben Überblick in der Buchreihe Teaming with microbes (Lowenfels und Lewis 2016) erhalten oder einen sehr tiefen, exakten im Review (Goswami et al. 2016). Das Review von Goswami et al. Enthält alle benötigten Referenzen, die für die einzelnen Nachweise notwendig sind, eigentlich gehören diese für einen perfekten Zitationsstil einzeln aufgelistet, aber dazu fehlt mir die Zeit, bitte einfach in den jeweiligen Kapiteln nachschauen.
Direkte Mechanismen:
Biologische Stickstofffixierung
Biologische Stickstofffixierung ist der Prozess, bei dem atmosphärisches Stickstoffgas (N2) in eine Ammoniumform (NH4+) umgewandelt wird, die von Pflanzen genutzt werden kann. Da Stickstoff ein wesentlicher Bestandteil des Pflanzenwachstums ist, aber in den meisten Böden nicht ohne weiteres verfügbar ist, ist dieser Prozess von entscheidender Bedeutung.
Stickstofffixierung ist die Methode, die von PGPR-Bakterien zur Stickstofffixierung verwendet wird, darunter Rhizobium spp. und Bradyrhizobium spp. Dieser Vorgang findet in spezialisierten Organen statt, die als Knöllchen bekannt sind und sich an den Wurzeln einiger Pflanzen, wie z. B. Leguminosen, entwickeln. Mit Hilfe eines Enzyms, der Nitrogenase, wandeln die PGPR-Bakterien in diesen Knöllchen Stickstoffgas in eine verwertbare Form um.
Lösung des nicht pflanzenverfügbaren Phosphors
Durch den Prozess der Phosphat-Solubilisierung wird Phosphat (PO4 3-) besser löslich und damit für Pflanzen besser verfügbar. Obwohl Phosphat ein wichtiger Pflanzennährstoff ist, liegt es in Böden häufig in einer unzugänglichen Form vor, z. B. als anorganisches Phosphat.
Anorganische Phosphate können von PGPR-Bakterien wie Bacillus- und Pseudomonas-Arten durch die Produktion organischer Säuren wie Zitronen- und Apfelsäure aufgelöst werden. Die Bakterien setzen diese organischen Säuren frei, die mit den anorganischen Phosphaten ein Chelat bilden und deren Löslichkeit in Wasser erhöhen können. Dadurch können die Pflanzen die Phosphate leichter aufnehmen und sie für ihr Wachstum und ihre Entwicklung nutzen.
Pseudomonas und Bacillus Arten, die organischen Phosphor lösen, sind in der Lage, Phosphor aus Phytat (In Mist und Kompost enthalten) und anderen Phospholipiden zu entfernen. Die anorganischen Phosphate stehen dann der Pflanzen zur Verfügung, nachdem die Bakterien die organischen Formen des Phosphors abgebaut haben.
Auch hier wird das ganze wieder über die Exkretion von Zitronen- und Apfelsäure Verbindungen gelöst. Andere Mechanismen wie Proton Exkretion durch Ammonium (NH4+) Ansammlung ist auch möglich, aber von der Funktionsweise unterscheidet sich die Methoden nur begrenzt, da die organischen Säuren auch nur als Protonendonor fungieren. (Park et al. 2009)
Produktion von Phytohormonen
Auch Phytohormone werden von PGPRs synthetisiert. Diese dienen als Pflanzenwachstumsregulatoren oder im englischen PGRs, welche zur Steuerung des Pflanzenwachstums beitragen. Je nach gewünschter Beeinflussung, kann eine andere PGPR-Art entweder natürlich angezüchtet und supplementiert werden oder als im Labor isoliert und zugegeben werden. Hiermit kann z.B. ein stauchender Effekt durch Cytokinene induziert werden.
Es folgt eine Liste von Phytohormonen, die von verschiedenen PGPRs produziert werden:
- Auxine: Es wurde festgestellt, dass PGPRs wie Pseudomonas fluorescens, Pseudomonas putida und Rhizobium leguminosarum Auxine produzieren, die für die Zelldehnung und -differenzierung verantwortlich sind. Sie fördern auch die Entwicklung der Seitenwurzeln und die Reifung der Früchte.
- Cytokinine: Es wurde festgestellt, dass PGPR wie Bacillus amyloliquefaciens, Bacillus subtilis und Azospirillum brasilense Cytokinine produzieren, die für die Zellteilung und die Entwicklung von Wurzeln, Sprossen und Blättern verantwortlich sind. Sie fördern auch die Entwicklung von Seitenwurzeln, die Reifung von Früchten und die Entwicklung von Chloroplasten.
- Gibberelline: Es wurde festgestellt, dass PGPR wie Pseudomonas fluorescens, Pseudomonas putida und Rhizobium leguminosarum Gibberelline produzieren, die für die Zellstreckung und -differenzierung verantwortlich sind. Sie fördern auch die Samenkeimung und das Sprosswachstum.
- Abscisinsäure: Einige PGPR wie Azospirillum brasilense produzieren Abscisinsäure, die für die Auslösung der Keimruhe und der Samenreifung verantwortlich ist und die Toleranz der Pflanzen gegenüber Umweltstress fördert.
- Jasmonate: Von einigen PGPR wie Pseudomonas syringae wurde berichtet, dass sie Jasmonate produzieren, bei denen es sich um Phytohormone handelt, die an der Abwehrreaktion der Pflanzen beteiligt sind.
Indirekte Mechanismen:
- Produktion von Siderophoren
Siderophore sind winzige, eisenbindende Substanzen, die von Mikroorganismen wie spezielle Bakterien gebildet werden und die ihnen helfen, Eisen aus ihrer Umgebung aufzunehmen. Um die Aufnahme von Eisen aus dem Boden zu unterstützen, sind mehrere pflanzenwachstumsfördernde Rhizobakterien (PGPR) in der Lage, Siderophore zu bilden.
- Pyoverdine, eine von Pseudomonas spp. produzierte Substanz, die Eisen aus eisenhaltigen Mineralien wie Eisenoxiden und -hydroxiden auflösen kann,
- Die Produktion von Bacillibactin durch Bacillus spp. ermöglicht es den Bakterien, Eisen zu chelatieren und zu nutzen.
Durch die Bildung von Siderophoren, die auch andere Mikronährstoffe aus dem Boden lösen können, beeinflussen einige PGPR nachweislich auch die Verfügbarkeit anderer Mikronährstoffe wie Zink und Mangan, die in Bezug auf Löslichkeit und Aufnahme durch Pflanzen mit Eisen vergleichbar sind. (Płociniczak et al. 2013)
- Chitinase- und Glucanase-Produktion durch PGPR
Chitinase und Glucanase sind beides Arten von zellwandabbauenden Enzymen, die von pflanzenwachstumsfördernden Rhizobakterien (PGPR) produziert werden. Chitinase ist ein Enzym, das die Chitin-Komponente der Zellwände von Pilzen abbaut, während Glucanase die Beta-Glucane abbaut, die in den Zellwänden verschiedener Organismen, einschließlich Pilzen und Bakterien, vorkommen.
Ein Beispiel für ein Bakterium, das Chitinase produziert, ist das im Boden lebende Pseudomonas aeruginosa, dass nachweislich Chitinase produziert, wenn es in Gegenwart von Chitin wächst. Ein weiteres Beispiel ist Bacillus subtilis, von dem bekannt ist, dass er sowohl Chitinase als auch Glucanase produziert.
Wenn PGPR Chitinase und Glucanase produzieren, können sie die Zellwände von Krankheitserregern wie dem Pilz Fusarium und anderen potenziellen Pflanzenpathogenen, die Chitin oder Beta-Glucane in ihren Zellwänden haben, abbauen. Dies kann zu einer Unterdrückung von pathogenen Infektionen in den Wurzeln und der Rhizosphäre von Pflanzen führen.
Darüber hinaus können diese Enzyme auch die Zellwände von nicht-pathogenen Mikroorganismen und organischen Stoffen im Boden abbauen. Dadurch können pflanzenverfügbare Nährstoffe wie Phosphor, Stickstoff und andere Mikronährstoffe aus den abgebauten Zellwänden freigesetzt werden, die von den Pflanzen verwertet werden können.
Darüber hinaus können die von der Chitinase produzierten Chitinfragmente bei Pflanzen eine systemisch erworbene Resistenz (SAR) auslösen, die ein wichtiger Mechanismus der Pflanzenimmunität gegen pathogene Infektionen ist und ein eigenes Kapitel erhält. (Chet et al. 1990)
Insgesamt ist die Produktion von Chitinase und Glucanase durch PGPR ein Schlüsselmechanismus, durch den diese Bakterien das Wachstum und die Gesundheit von Pflanzen fördern können, indem sie die Verfügbarkeit von Nährstoffen erhöhen und pathogene Infektionen unterdrücken.
- Antibiotika-Produktion durch PGPR
Bei einem Prozess, der als "Antibiotikaerzeugung durch pflanzenwachstumsfördernde Rhizobakterien" (PGPR) bekannt ist, produzieren bestimmte Bakterien Substanzen mit antibakteriellen Eigenschaften. Diese Stoffe können die Pflanzenentwicklung und die Nährstoffaufnahme fördern und gleichzeitig dazu beitragen, die Pflanzen vor Krankheiten zu schützen.
Biosynthese und Sekretion sind die beiden wichtigsten Prozesse, durch die PGPR-Antibiotika erzeugen können. Bei der Sekretion geben die Bakterien das Antibiotikum an die Umwelt ab, während bei der Biosynthese die Bakterien das Antibiotikum aktiv in ihren eigenen Zellen synthetisieren.
Das Bakterium Streptomyces griseus ist ein Beispiel für eine PGPR, die Antibiotika synthetisiert. Zahlreiche Antibiotika, wie Griseofulvin und Streptomycin, werden von diesem Bakterium produziert. Ein weiteres Beispiel ist das Bakterium Pseudomonas fluorescens, von dem bekannt ist, dass es die antibiotischen Chemikalien Phenazine-1-carboxamide (PCN) und Pyoluteorin (Plt) produziert. (Hammer et al. 1997)
- Induzierte systemische Resistenz
Induzierte systemische Resistenz (ISR) ist ein Phänomen, bei dem die Anwendung bestimmter Mikroben, wie z. B. pflanzenwachstumsfördernde Rhizobakterien (PGPR), die natürlichen Abwehrmechanismen einer Pflanze aktivieren kann, was zu einer erhöhten Resistenz gegenüber Krankheitserregern führt. Dies ist eine wichtige Strategie zur Krankheitsbekämpfung bei Nutzpflanzen, da sie den Schutz der Pflanzen ohne den Einsatz chemischer Pestizide ermöglicht.
Es gibt mehrere Mechanismen, durch die PGPR eine systemische Resistenz in Pflanzen induzieren können. Einer der wichtigsten Mechanismen ist die Produktion von Signalmolekülen, die als Elicitoren der systemisch erworbenen Resistenz (SAR) bekannt sind, wie z. B. Salicylsäure (SA) und Jasmonsäure (JA). Diese Moleküle werden von den PGPR produziert und können die SAR-Reaktion der Pflanze aktivieren, was zu einer erhöhten Resistenz gegenüber Krankheitserregern führt.
Ein weiterer Mechanismus ist die Produktion von Enzymen wie Chitinasen, beta-1,3-Glucanasen und Peroxidasen. Diese Enzyme sind dafür bekannt, dass sie die Zellwände von Krankheitserregern abbauen und es ihnen so erschweren, die Pflanze zu infizieren. Zudem werden die Chitinfragmente, welche bei der Aufspaltung entstehen als PAMP (pathogen associated molecular pattern) erkannt. Dies ist eine Form von Marker anhand dessen die Pflanze ihre aktiven Abwehrmechanismen in Gang bringt (PTI = Pattern triggered immunity = Muster induzierte Immunität) (Couto und Zipfel 2016)
Ein Beispiel für einen PGPR-Stamm, von dem bekannt ist, dass er durch SAR-Auslösung eine systemische Resistenz induziert, ist das Bakterium Pseudomonas aeruginosa. Dieses Bakterium produziert eine Reihe von Molekülen, die SAR aktivieren können, darunter SA und JA. Ein weiteres Beispiel für einen PGPR-Stamm, von dem bekannt ist, dass er durch die Produktion von Enzymen eine systemische Resistenz auslöst, ist Bacillus subtilis, der Chitinasen, Beta-1,3-Glucanasen und Peroxidasen produziert. (Goswami et al. 2016)
- PGPR moduliert pflanzliche Stressmarker unter abiotischem Stress
Abiotischer Stress ist jeder Stress, dem eine Pflanze ausgesetzt ist und der nicht biologischer Natur ist, wie z. B. Trockenheit, hoher Salzgehalt oder raue Temperaturen. Diese Stressoren können die Expression bestimmter Gene verändern, was zu Stressindikatoren führt, mit denen sich das Ausmaß des Stresses messen lässt.
Unter abiotischen Stressbedingungen können PGPR die pflanzlichen Stressindikatoren durch eine Reihe verschiedener Methoden verändern. Die Bildung von Molekülen, die das Pflanzenwachstum fördern, wie Indolessigsäure (IAA) und Cytokinine, ist einer der Schlüsselprozesse. Diese Substanzen können dazu beitragen, die Auswirkungen von Stress zu mildern, indem sie das Pflanzenwachstum fördern und die Pflanze vor stressbedingten Schäden schützen.
Ein weiterer Mechanismus ist die Produktion von Enzymen wie Dehydrin, Prolin und dem antioxidativen Enzym Superoxid-Dismutase (SOD), die dazu beitragen können, die Pflanze vor stressbedingten Schäden zu schützen, indem sie die Zellmembran stabilisieren, die Denaturierung von Proteinen verhindern und die Produktion reaktiver Sauerstoffspezies (ROS) in der Pflanze verringern.
Ein Beispiel für einen PGPR-Stamm, von dem bekannt ist, dass er pflanzliche Stressmarker durch die Produktion von pflanzenwachstumsfördernden Verbindungen moduliert, ist das Bakterium Bacillus subtilis. Dieses Bakterium ist dafür bekannt, dass es IAA und Cytokinine produziert, die das Pflanzenwachstum fördern und die Pflanze vor stressbedingten Schäden schützen können. Ein weiteres Beispiel ist das Bakterium Pseudomonas putida, von dem bekannt ist, dass es die Enzyme Dehydrin und Prolin produziert, die zum Schutz der Pflanze vor stressbedingten Schäden beitragen können, indem sie die Zellmembran stabilisieren, die Denaturierung von Proteinen verhindern und die Produktion von ROS in der Pflanze verringern.
(Niu et al. 2012; Goswami et al. 2016; Rasool et al. 2013)
- Herstellung von 1-Aminocyclopropan-1-carbonsäure-Desaminase
1-Aminocyclopropan-1-carbonsäure (ACC)-Desaminase ist ein Enzym, das ACC, eine Vorstufe des Pflanzenhormons Ethylen, in Ammoniak und Alpha-Ketobutyrat umwandelt.
Die Produktion von ACC-Desaminase durch PGPRs ist ein gut dokumentierter Mechanismus bei der Regulierung des Pflanzenwachstums und der Stressreaktionen. ACC-Desaminase zerlegt ACC, ein Substrat des Pflanzenhormons Ethylen, in Ammoniak und Alpha-Ketobutyrat. Dadurch wird der Ethylenspiegel wirksam gesenkt. Ethylen ist ein Hormon, das bekanntermaßen eine hemmende Wirkung auf das Pflanzenwachstum hat und auch mit Stressreaktionen in Verbindung gebracht wird. (Etesami et al. 2015)
Ein Beispiel für PGPR, die ACC-Deaminase produzieren, ist Pseudomonas spp. Diese Bakteriengruppe produziert ACC-Deaminase und hat nachweislich wachstumsfördernde Wirkungen auf eine Vielzahl von Pflanzenarten.
Ein weiteres Beispiel ist das Bakterium Burkholderia spp., das Berichten zufolge ACC-Deaminase produziert und nachweislich das Wachstum fördert und die Toleranz von Pflanzen gegenüber verschiedenen abiotischen Stressfaktoren wie Trockenheit und hohen Salzkonzentrationen verbessert.
Archae
Mikroorganismen mit einer einzigen Zelle gehören zum Bereich der Archaeen. Sie sind eine vielfältige Gruppe von Lebewesen, die sich sowohl chemisch als auch genetisch von Bakterien und Eukaryoten (den beiden anderen Lebensbereichen) unterscheiden.
Archaeen sind in einer Vielzahl von Umgebungen zu finden, darunter auch in rauen Umgebungen wie Salinen, heißen Quellen und hydrothermalen Schloten in der Tiefsee. Außerdem sind sie in gemäßigteren Umgebungen wie dem Boden und dem Meer zu finden.
Sowohl Bakterien als auch Archaeen sind wichtige Bestandteile der Bodenmikroflora und haben einen erheblichen Einfluss auf die Bodenprozesse, die das Pflanzenwachstum und die Pflanzengesundheit beeinflussen. Beide Arten von Mikroben können das Pflanzenwachstum beeinflussen, indem sie organisches Material zersetzen und Nährstoffe freisetzen, die von den Pflanzen aufgenommen werden können, die Entwicklung einer günstigen Bodenstruktur fördern und als Barriere gegen Krankheitserreger wirken.
Einer der Hauptunterschiede zwischen Archaeen und Bakterien ist der Prozess der Energiegewinnung. Während viele Bakterien den Sauerstoff bei der Atmung zur Energiegewinnung nutzen, sind Archaeen oft anaerob und erzeugen Energie durch einen Prozess, der als Methanogenese bekannt ist. Methan ist das Ergebnis des Stoffwechsels von Methanogenen, bei denen es sich um Archaeen handelt. Dadurch kann der Kohlenstoffkreislauf in Böden erheblich beeinflusst werden, und Methanogenese kann nach einigen Forschungsergebnissen sogar zu einer erhöhten Bodenfruchtbarkeit beitragen.
Die Art und Weise, wie Bakterien und Archaeen mit Pflanzen interagieren, ist ebenfalls unterschiedlich. Während einige Bakterien nachweislich direkte wechselseitige Beziehungen zu Pflanzen unterhalten, indem sie beispielsweise Stickstoff in Knöllchen an den Wurzeln von Hülsenfrüchten binden oder das Pflanzenwachstum durch die Produktion entsprechender Chemikalien unterstützen, ist dies bei Archaeen in der Regel nicht der Fall. Archaeen können auch an der Entwicklung von Biofilmen auf Pflanzenwurzeln beteiligt sein, die zum Schutz der Pflanzen vor Krankheiten beitragen können. Einige Archaeen erzeugen nachweislich flüchtige organische Chemikalien wie methanol oder formaldehyd produzieren, die das Pflanzenwachstum durch verbesserte Nährstoffverfügbarkeit stimulieren können.
Zudem sind sie im Schwefelzyklus beteiligt. Sie oxidieren Schwefel und produzieren Schwefelsäure damit, welche Mineralstoffe aus Steinen lösen können. Calcium kann z.B. so zu Calciumsulfat umgewandelt werden, wenn calciumhaltige Verbindungen bereitstehen. Dieser Stoff wird gemein hin als Gips bezeichnet und bietet sowohl gute Belüftung durch seine Porenstruktur als auch eine Nährstoffquelle beim Zerfall. (Lin et al. 2010; Naitam und Kaushik 2021)
Mikro Fauna
Bevor wir in die genauen Aufgaben der Bodenlebewesen gehen, müssen wir eine Einteilung gemäß ihrer Aufgaben festlegen.
Die sogenannten Nekrotrophen, ernähren sich von toten oder verrottenden Substanzen. Sie sind entscheidend für den Abbauprozess, der dazu beiträgt, dass Nährstoffe wieder in das Ökosystem zurückgeführt werden. Sie töten aktiv die Pflanze, um an das tote Gewebe zu kommen.
Mikroben, die sich von Lebewesen ernähren, werden als Biotrophe bezeichnet. Mit Pflanzen, Tieren und anderen Arten gehen sie häufig symbiotische Partnerschaften ein, bei denen jeder im Austausch für den anderen einen Nutzen erhält.
Je nach Ressourcenangebot können fakultative Mikroorganismen entweder in lebenden oder toten Substanzen existieren. Je nach Umgebung können sie als Nekrotrophe oder Biotrophe auftreten.
Mikroorganismen, die sich nur von schon bereits toten oder verrottenden Substanzen ernähren, werden als saprophytische Mikroorganismen bezeichnet. Sie sind von entscheidender Bedeutung für den Abbauprozess, der dazu beiträgt, dass Nährstoffe wieder in das Ökosystem zurückgeführt werden. Bakterien, Pilze und verschiedene Algenarten sind einige Beispiele für saprophytische Mikroorganismen. (Agrios 2005)
Algen
Der Einfluss von Algen und deren produzierten Stoffen im Boden sind bereits seit den 1960gern bekannt und bedingte Nachforschungen wurden bereits aufgestellt. Das Review von (Dmytryk und Chojnacka 2018) gibt einen sehr guten Überblick über deren Eignung als Produzent von Biostimulanzien und Einsatz als Pflanzenstärkungsmittel.
Die als Algen bekannten Wasserorganismen sind eine vielfältige Kategorie, die sowohl einfache einzellige Organismen als auch komplexe mehrzellige Formen umfasst. Sie unterscheiden sich von Pflanzen, Tieren und Pilzen und werden dem Reich der Protista zugeordnet. Es gibt viele verschiedene Arten von Lebensräumen, in denen Algen vorkommen, darunter Süßwasser-, Meeres- und Land-Ökosysteme. Sie können ihre eigene Nahrung herstellen, da sie photosynthetisch sind, d. h., dass Lichtenergie während des Prozesses der Photosynthese in chemische Energie umgewandelt wird.
Algen spielen eine wichtige Rolle beim Abbau organischer Abfälle und beim Nährstoffkreislauf im Boden-Kompostkreislauf. Durch die Absonderung von Enzymen, die komplizierte Verbindungen abbauen, können Algen im Komposthaufen den Abbau von organischem Material beschleunigen.
Außerdem können sie Nährstoffe, die für das Pflanzenwachstum wichtig sind, wie Stickstoff, Phosphat und Kalium, aufnehmen und speichern.
Anbei eine Liste aus dem Paper (Dmytryk und Chojnacka 2018) zur Übersicht, ich werde hier jetzt nichtmehr genau auf jeden Stoff eingehen.
Abbildung 24: Die Wirkung der von Algen produzierten Poly- und Oligosacchariden bei der Anwendung auf Pflanzen (Dmytryk und Chojnacka 2018)

Abbildung 25: Die Wirkung von Phytohormonen und hormonähnlichen Verbindungen bei der Anwendung auf Pflanzen (Dmytryk und Chojnacka 2018)
Pilze (PGPFs)
Der nächsten riesige Bestandteil von Bodenmikroorganismen sind die Pilze. Hierbei gibt es auch eine Vielzahl an verschiedenen Wirkmechanismen. Das ganze Thema vollständig abzubilden, wird auch hier wieder in der kurzen Zeit sehr schwierig. Ich empfehle auch hier wieder einen Review Artikel:
Eine vielfältige Gruppe von Pilzen, die als pflanzenwachstumsfördernde Pilze (plant growth-promoting fungi, PGPFs) bekannt sind, interagiert symbiotisch mit Pflanzen. Sie siedeln sich in den Wurzeln an und sind entscheidend für die Entwicklung der Pflanzen, die Nährstoffaufnahme und die Toleranz gegenüber biotischen und abiotischen Stressfaktoren. Viele Stämme, wie die Glomeromycota, Ascomycota und Basidiomycota, enthalten PGPFs.
Glomeromycota
Der Stamm der Glomeromycota ist dafür bekannt, dass er eine wichtige Rolle bei der Entwicklung von arbuskulären Mykorrhizabindungen (AM) mit Pflanzen spielt.
Es gibt zwei Arten von Mykorrhiza Pilzen, einmal Endo- und Ektomykorrhiza. Wir benötigen die Endo Variante da diese mit Gräsern und Nutzpflanzen symbiotische Bindungen eingeht. Die Ekto Stämme findet man an Bäumen wie z.B. den gemeinen Steinpilz bei Fichten. Sie siedeln sich auf der Oberfläche der Wurzeln an und können Fruchtkörper ausbilden.
Im Gegensatz dazu findet man die von uns benötigten arbuskulären endo-Mykorrhizapilze in einer Zwischenschicht der Wurzel. Hier wachsen sie fest und bilden sozusagen eine Andockstation. Von dieser aus, erweitert sich der Pilz nach außen und bildet baumartig aussehende Hyphae (Ketten an Pilzzellen, wie kleine Wurzeln). Dies ist auch der Namensursprung der arbuskulären Mykorrhizapilze, denn Arbus kommt aus dem Lateinischen und bedeutet Baum.
Abbildung 26: Arbuskulärer Arm des Pilzes wächst ins Zell Lumen (Remy et al. 1994)
Diese Pilze verbessern die Nährstoffaufnahme und helfen den Pflanzen bei der Bewältigung von biotischem und abiotischem Stress, indem sie die Wurzelzellen der meisten Pflanzen besiedeln. Dies erhöht die Wurzeloberfläche und fördert damit sowohl die Wasser als auch die Phosphoraufnahme beträchtlich in Kombination mit der Freisetzung von organischen Säuren und Phosphatasen. Der Einzugsradius Phosphors wurde von mehreren mm auf bis zu 11cm erhöht (JAKOBSEN et al. 1992). Dies statistisch signifikant und essenziell für den optimalen Ertrag im Living soil System.
Rhizophagus irregularis, früher bekannt als Glomus intraradices und der sehr prominente Glomus mossae, sind Beispiele für PGPF-Stämme, die das Wachstum einer Vielzahl von Nutzpflanzen, einschließlich Sojabohnen, Hanf und Tomaten fördern. (Błaszkowski 1994; Bever et al. 2001)
Ascomycota
Ascomycota ist ein Stamm, der eine große Vielfalt von Pilzen umfasst, von denen viele nachweislich PGP-Eigenschaften haben. Ein Beispiel für einen PGPF aus diesem Stamm ist Trichoderma spp., der das Pflanzenwachstum fördern kann, indem er Enzyme produziert, die komplexe organische Moleküle abbauen und wachstumsfördernde Substanzen wie Indolessigsäure (Auxin-Hormon) freisetzen. Trichoderma kann auch die Toleranz der Pflanzen gegenüber Umweltbelastungen verbessern und die pflanzlichen Abwehrmechanismen gegen Krankheitserreger stärken (ISR -> siehe Kapitel 2.3.2.1 indirekte Mechanismen).
Trichoderma ist ebenfalls dafür bekannt, eine Vielzahl von Enzymen zu produzieren, darunter Cellulasen, Chitinasen, Proteasen und Cellulasen (CWDEs = cell wall degrading enzymes), die die Zellwände anderer Pilze hydrolysieren können und ihnen einen Wettbewerbsvorteil gegenüber anderen Pilzkrankheiten verschaffen. Diese Enzyme können den Abbau von organischem Material unterstützen und Nährstoffe für die Pflanzenaufnahme freisetzen.
Es ist auch wichtig zu wissen, dass verschiedene Trichoderma-Arten unterschiedliche Fähigkeiten zur Pflanzeninfektion haben. Trichoderma virens und Trichoderma koningii zum Beispiel sind als pathogen bekannt und können Pflanzen schädigen, während Trichoderma harzianum und Trichoderma asperellum das Pflanzenwachstum fördern.
Basidiomycota
Basidiomycota ist ein weiterer Stamm, der eine Vielzahl von Pilzen, darunter auch Champignons, umfasst. Ein Beispiel für einen PGPF aus diesem Stamm ist Laccaria bicolor, der das Pflanzenwachstum fördern kann, indem er die Nährstoffaufnahme verbessert und die Toleranz der Pflanzen gegenüber Umweltstress erhöht. Dieser Pilz kann auch Enzyme produzieren, die komplexe organische Moleküle abbauen, und es hat sich gezeigt, dass er das Wachstum und die Wurzelbiomasse bei einer Reihe von Pflanzen erhöht.
Wen weitere Fakten und Kulturspezifische Eigenschaften der Stämme interessieren, sollte unbedingt das Review (Hossain et al. 2017) und (Devi et al. 2020) lesen.
Nematoden
Entomopathogene Nematoden (EPN), die gemeinhin als nützliche Nematoden bezeichnet werden, sind eine Vielzahl von Rundwürmern, die im Boden leben. Sie sind dafür bekannt, dass sie zur Bodenverbesserung beitragen, Krankheitserreger hemmen und die Pflanzenentwicklung fördern.
Nützliche Nematoden gibt es in einer Vielzahl von Formen, jede mit ihren eigenen besonderen Eigenschaften und Wirkungsweisen. Die beiden Gattungen, die am häufigsten in der biologischen Schädlingsbekämpfung eingesetzt werden, sind Steinernema und Heterorhabditis. Diese Nematoden sind dafür bekannt, dass sie eine Vielzahl von wirbellosen Tieren und bodenbewohnenden Insekten, darunter Termiten, Madenwürmer und Engerlinge, befallen und töten. Durch natürliche Öffnungen wie den Mund, den Anus oder die Atmungsporen infizieren sie ihren Wirt. Sobald sie in ihrem Inneren sind, setzen sie für sie symbiotische Bakterien frei, die den Wirt zerstören.
Diese Nematoden sind dafür bekannt, dass sie die Bodengesundheit verbessern, indem sie die Insektenpopulationen reduzieren und die Nährstoffverfügbarkeit erhöhen.
Pflanzenpathogene Nematoden können durch einige nützliche Nematoden unterdrückt werden, darunter Arten der Gattung Phasmarhabditis. Bekannte pflanzenparasitische Nematoden wie der Wurzelknöterich und die Dolchstichnematode können von diesen Würmern infiziert und abgetötet werden. Bei der Bekämpfung pflanzenparasitärer Nematoden im Boden können sie als biologische Bekämpfungsmittel eingesetzt werden.
Da es so viele verschiedene Nutzzwecke gibt, kann man die Nematoden anhand ihrer Vorgehensweise charakterisieren.
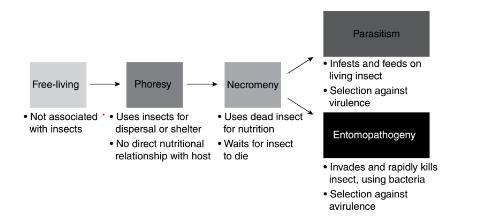
Abbildung 27: Systematik Nematoden (Abd-Elgawad et al. 2017)
Auch hier gilt wie bei den letzten Kapiteln: Reviews lesen und eigene Meinung bilden (Abd-Elgawad et al. 2017) Kapitel 1-3 sollten hierfür geeignet sein.
Des Weiteren gibt es eine genau Auflistung der geeigneten Wirte für die oben angesprochenen Nematodenarten. Es gilt jedoch dabei zu beachten insbesondere, wenn man ein nicht komplett geschlossenes System hat, dass man nur „heimische“ Arten verwendet. Erstens für den Nachhaltigkeitsgedanken, den man zumindest halbwegs haben sollte und zweitens aufgrund der Invasiven Natur mancher Arten, die hier aufgelistet sind.
Abbildung 28: Geeignete Wirte (Insekten) für Steinernema und Heterorhabditis sp. (Abd-Elgawad et al. 2017)
Protozoen
Protozoen sind eine vielfältige Gruppe von Einzellern, die eine entscheidende Rolle im Nahrungsnetz des Bodens spielen. Sie können in mehrere Gruppen eingeteilt werden, darunter Amöben, Wimpertierchen und Flagellaten, die jeweils unterschiedliche Merkmale und ökologische Funktionen haben.
Im Boden verzehren Protozoen Bakterien, Pilze und andere Mikroorganismen und regulieren so deren Populationen. Dieser Verzehr wirkt sich wiederum auf die Verfügbarkeit von Nährstoffen wie Nitraten und Phosphaten für Pflanzen aus. Darüber hinaus können Protozoen auch Nährstoffe aus organischem Material freisetzen, wodurch diese für die Pflanzen besser verfügbar werden. So sind beispielsweise Amoeba spp. und Vorticella spp. dafür bekannt, dass sie eine wichtige Rolle bei der Zersetzung von organischem Material und der Freisetzung von Nährstoffen spielen.
Aber auch Hormonelles Feedback wird an die Pflanze gesendet. Auxin z.B. in Form von IAA, welches für das apikale Wachstum (Wachstum entlang der Spitze) der Wurzeln verantwortlich ist, wird freigesetzt und der Pflanze damit suggeriert, dass sie in diese Richtung weiter expandieren kann, da Protozoen also Nährstoffversorgung gegeben sind.
Abbildung 29: "Ein konzeptionelles Modell zur Veranschaulichung der hormonellen Auswirkungen der Mikrofauna auf das Wurzelwachstum, modifiziert nach Bonkowski & Brandt (2002). Wurzelausscheidungen (1) stimulieren das Wachstum einer vielfältigen Bakteriengemeinschaft (Bonkowski 2004)
Protozoen spielen auch eine Rolle bei der Bekämpfung von Pflanzenpathogenen. Einige Arten, wie z. B. Rhizomonas spp., verzehren Bakterien, die Pflanzenkrankheiten verursachen können, und helfen so, die Pflanzen vor Infektionen zu schützen.
Ein Beispiel für spezifische Arten, die eine entscheidende Rolle im Nahrungsnetz des Bodens spielen, ist die Gattung Tetrahymena. Es handelt sich dabei um Wimpertierchen, die die Fähigkeit haben, Zellulose in Pflanzenmaterial abzubauen, um sie für die Pflanzenaufnahme verfügbar zu machen und das Pflanzenwachstum zu fördern. Diese Fähigkeit macht Tetrahymena zu einem wertvollen Bio-Dünger für die nachhaltige Landwirtschaft.
Protozoen lassen sich aufgrund ihrer Eigenschaften und ökologischen Rolle in mehrere Kategorien einteilen. Im Folgenden finden Sie einige der Hauptgruppen von Protozoen, Beispiele für Arten innerhalb jeder Gruppe und Beispiele dafür, wie sie nachweislich das Nahrungsnetz im Boden und/oder das Pflanzenwachstum beeinflussen:
- Amöben: Amöben sind einzellige Organismen, die sich mit Hilfe von Pseudopodien fortbewegen und eine wichtige Rolle bei der Zersetzung von organischem Material und der Freisetzung von Nährstoffen spielen. Beispiele für Amöben, die nachweislich das Nahrungsnetz im Boden und/oder das Pflanzenwachstum beeinflussen, sind Acanthamoeba spp. und Dictyostelium discoideum. Acanthamoeba spp. beispielsweise verzehren nachweislich Bakterien und Pilze und regulieren so deren Populationen; außerdem setzen sie Nährstoffe aus organischem Material frei, so dass diese besser für die Pflanzenaufnahme verfügbar sind. Dictyostelium discoideum ist nachweislich ein Bodenprotozoon, der das Pflanzenwachstum durch Freisetzung von Phosphor aus organischem Material fördert.
- Wimpertierchen: Ciliaten sind einzellige Organismen, die sich durch das Vorhandensein von Flimmerhärchen auszeichnen, die sie zur Fortbewegung nutzen. Beispiele für Ciliaten, die nachweislich das Nahrungsnetz im Boden und/oder das Pflanzenwachstum beeinflussen, sind Tetrahymena spp. und Rhizomonas spp. Tetrahymena spp. baut nachweislich Zellulose in Pflanzenmaterial ab, macht sie für die Pflanzenaufnahme verfügbar und fördert so das Pflanzenwachstum; außerdem spielt es eine Rolle bei der Zersetzung organischer Stoffe und der Freisetzung von Stickstoff und Phosphor. Rhizomonas spp. verzehren nachweislich Bakterien, die Pflanzenkrankheiten verursachen können, und tragen so zum Schutz der Pflanzen vor Infektionen bei.
- Flagellaten: Flagellaten sind einzellige Organismen, die sich durch das Vorhandensein von Geißeln auszeichnen, die sie zur Fortbewegung nutzen. Beispiele für Flagellaten, die nachweislich das Nahrungsnetz im Boden und/oder das Pflanzenwachstum beeinflussen, sind Vorticella spp. und Colpoda spp. Es wurde festgestellt, dass Vorticella spp. Bakterien verzehrt und so deren Populationen reguliert, und es wurde auch festgestellt, dass sie Stickstoff und Phosphor im Boden freisetzt, so dass diese für die Pflanzenaufnahme besser verfügbar sind. Colpoda spp. spielt nachweislich eine Rolle im Nährstoffkreislauf, indem es organisches Material abbaut und Nährstoffe freisetzt.
Würmer
Regenwürmer, die zum Stamm der Ringelwürmer (Annelida) gehören, spielen eine entscheidende Rolle im Nahrungsnetz des Bodens, indem sie die Bodenstruktur verbessern, den Boden belüften, seine Wasserhaltekapazität erhöhen und Nährstoffe recyceln. Sie werden in drei Hauptgruppen eingeteilt: epigäische, endogäische und anökische Regenwürmer, die jeweils einzigartige Merkmale und ökologische Funktionen haben. (Palm et al. 2013)
Regenwürmer sind dafür bekannt, dass sie große Mengen an Boden und organischem Material verzehren, wodurch sie den Boden durchmischen und belüften und seine Porosität und Wasserhaltefähigkeit erhöhen. Dies verbessert die Bodenstruktur und die Fruchtbarkeit, was wiederum dem Pflanzenwachstum zugutekommt. Allerdings ist dies auch wieder vom Boden selbst abhängig. Wurmverdauung verbesserte zwar die neuen Polyvalenten Bindungen, aber löst auch zu einem gewissen Grad die Tonbindungen im Boden. D.h. je höher den Tonanteil des Bodens, desto weniger signifikant wird die Verbesserung der Bodenstruktur. (Schrader und Zhang 1997) Bei uns im Torf ist dies aber durch die Abwesenheit des Tons irrelevant und es kann gesagt werden, dass Wurmhumus generell die Struktur verbessert.
Einer der wichtigsten Beiträge der Regenwürmer zum Nährstoffkreislauf ist ihr Verdauungssystem, ein komplexer Prozess, der die Freisetzung von Enzymen und Mikroben beinhaltet. Der Darm des Regenwurms enthält verschiedene Enzyme, die organisches Material abbauen, darunter Cellulase, die Zellulose abbaut, und Protease, die Proteine abbaut. Der Regenwurmdarm enthält auch eine vielfältige Gemeinschaft von Mikroben, darunter Bakterien und Pilze, die die organische Substanz weiter abbauen.
Der Abbau von organischem Material durch Regenwürmer führt zur Freisetzung verschiedener Nährstoffe wie Stickstoff, Phosphor und Kalium, die im Regenwurmdarm chelatisiert werden. Chelatierte Nährstoffe sind Mineralien, die an organische Moleküle gebunden sind, so dass sie von den Pflanzen besser aufgenommen werden können. Dieser Prozess erfolgt durch die Wirkung von Enzymen, sogenannten Chelatbildnern, die von den Regenwürmern oder ihren Darmmikroben produziert werden. Zu diesen Chelatbildnern gehören Siderophore und Phytosiderophore, die Eisen chelatisieren, sowie organische Säuren wie Citrat, Gluconat und Oxalat, die andere Metalle wie Zink und Mangan chelatisieren.
Epigäische Regenwürmer wie Eisenia fetida (Rotwurm) leben an der Oberfläche des Bodens und zersetzen hauptsächlich organische Stoffe. Sie werden häufig in Kompostierungssystemen eingesetzt, wo sie organische Abfälle effizient abbauen und die Bodenfruchtbarkeit verbessern, was dem Pflanzenwachstum zugutekommt.
Endogeische Regenwürmer, wie z. B. Aporrectodea spp, sind Wühler, die im Ober- und Unterboden leben. Sie legen horizontale Gänge an und verbessern die Bodenstruktur, indem sie organisches Material und Mineralboden vermischen, was die Wasserinfiltration und die Belüftung fördern. Außerdem tragen sie zum Nährstoffkreislauf bei, indem sie organisches Material abbauen und Nährstoffe freisetzen, insbesondere Phosphor und Stickstoff, die für das Pflanzenwachstum wichtig sind.
Anökische Regenwürmer wie Lumbricus terrestris legen tiefe vertikale Gänge im Boden an, die die Bodenstruktur verbessern, indem sie die Porosität und die Wasserinfiltration erhöhen, und sie bringen auch tiefer liegende Nährstoffe näher an die Oberfläche. Ihre Höhlen dienen auch als Drainagekanäle und verbessern die Sauerstoffversorgung des Bodens.
In Bodensystemen in Innenräumen können epigeische und endogene Regenwürmer für den Abbau organischer Stoffe und die Verbesserung der Bodenfruchtbarkeit nützlich sein, während anökische Regenwürmer die Bodenstruktur und die Belüftung verbessern können. Durch den Einsatz einer Kombination von Regenwurmarten können Bodensysteme in Innenräumen von den vielfältigen ökologischen Nischen und Funktionen der verschiedenen Regenwurmgruppen profitieren, was wiederum zu einem besseren Pflanzenwachstum führen kann.
Abbildung 30: Beteiligung der Würmer an der Pedogenese (Bodenbildung) (Babu Ojha und Devkota 2014)
Es ist zu beachten, dass die Regenwurmpopulationen und -vielfalt je nach Innenraumsystem und den angewandten Bewirtschaftungsmethoden variieren können. Außerdem ist es wichtig, dass optimale Feuchtigkeits-, Temperatur- und Lichtbedingungen herrschen, damit der Regenwurm überleben und gedeihen kann. Außerdem sollte man die Auswirkungen der Anwendung von Pestiziden oder andere Chemikalien, die der Regenwurmpopulation schaden könnten, beachten.
Neben ihren positiven Auswirkungen auf die Bodenstruktur und -fruchtbarkeit können Regenwürmer auch eine wichtige Rolle bei der Regulierung der mikrobiellen Gemeinschaften im Boden spielen. Regenwürmer ernähren sich nachweislich selektiv von bestimmten Arten von Mikroorganismen und fördern das Wachstum nützlicher Bakterien, die die Bodengesundheit und das Pflanzenwachstum verbessern können.
Genauere Informationen findet ihr wie immer selbst bei google scholar oder spezifisch im Review von (Lavelle 1988) oder (Edwards und Arancon 2004)
Arthropoden (Gliederfüßer)
Arthropoden sind eine vielfältige Gruppe von Tieren, zu denen Insekten, Spinnen, Krebstiere und Tausendfüßler gehören. Sie spielen eine wichtige Rolle im Nahrungsnetz des Bodens und dienen als Zersetzer, Räuber und Beute. Sie haben verschiedene ökologische Funktionen und können erhebliche Auswirkungen auf die Bodengesundheit und das Pflanzenwachstum haben, insbesondere in lebenden Bodensystemen in Innenräumen.
Zu den Arthropoden, die für das Soil food web wichtig sind, gehören verschiedene Insektengruppen, wie Käfer, Springschwänze und Milben. Innerhalb dieser Gruppen gibt es viele verschiedene Arten, die unterschiedliche Auswirkungen auf die Bodengesundheit und das Pflanzenwachstum haben können.
So spielen beispielsweise Käfer der Familie Scarabaeidae, wie der Gemeine Mistkäfer (Scarabaeus sp.), eine wichtige Rolle bei der Zersetzung von tierischen Abfällen und tragen zum Nährstoffkreislauf im Boden bei. Diese Käfer graben sich in den Dung ein und helfen dabei, ihn zu vergraben und zu zersetzen, was die Bodenstruktur und die Fruchtbarkeit verbessern. Allerdings wollen wir diese nicht in unserem Indoor-boden haben, da wir auch keine unkompostierten/bereits umgesetzten tierischen Produkte verwenden. Dies bäte nämlich einen perfekten Nährboden für Salmonella ssp. und andere Schadorganismen, die zwar nicht die Pflanze schädigen, jedoch für die Menschen toxisch sind. Dies würde sogar zu einem Durchfallen in den Reinheitstests der Blüten führen. (Deutscher Apotheker-Verlag Doktor Roland Schmiedel 2021; Kim und Jiang 2010)
Eine andere Gruppe, die Springschwänze (Collembola), sind winzige, flügellose Insekten, die im Boden häufig vorkommen. Sie sind effiziente Zersetzer und Räuber anderer Bodenorganismen und können zur Bekämpfung von Schädlingen und Krankheiten im Boden beitragen. Für spezifische Informationen zu diese Art, empfehle ich die Website, die wirklich mit Begeisterung gebaut wurde und echt schöne Bilder, wie dieses enthält (A Chaos of Delight 2023).
Abbildung 31: Weißer Springschwanz (A Chaos of Delight 2023)
Milben, vor allem aus der Familie der Oribatida, sind im Boden häufig anzutreffen und spielen eine wichtige Rolle beim Abbau organischer Stoffe sowie bei der Kontrolle von Schädlingspopulationen. Sie ernähren sich von abgestorbenem Pflanzenmaterial und Mikroorganismen, bauen diese ab, setzen Nährstoffe frei und tragen zum Aufbau organischer Substanz bei, was sich positiv auf das Pflanzenwachstum und die Bodengesundheit auswirken kann.
Durch unseren Indoor-Boden und die wechselnden Bedingungen von warm/feucht zu eher kühl/trocken im Laufe des Lebenszykluses der Pflanze, verändern Klimaspezifische Arthropoden Populationen.
Es gibt mehrere Arthropodengruppen und -arten, die spezifischunter heißen und feuchten Bedingungen gedeihen, darunter auch solche, die in torfhaltigen Böden vorkommen. So sind beispielsweise einige Springschwanzarten (Collembola) dafür bekannt, dass sie hohe Temperaturen und Feuchtigkeit vertragen und in Torfmooren und anderen Feuchtgebieten vorkommen. Auch bestimmte Milbenarten (Oribatida) sind in Torfböden verbreitet und können eine wichtige Rolle beim Abbau organischer Stoffe spielen.
Andere Arthropoden, die in tropischen, feuchten Umgebungen vorkommen, sind Rüsselkäfer (Staphylinidae), die als Zersetzer, Räuber und Beute eine Rolle im Nahrungsnetz des Bodens spielen können und in verschiedenen Lebensräumen, einschließlich Torfböden, zu finden sind.
Diese Gruppen gedeihen also besser in vegetativ, warm/feuchten, Bedingungen.
Andererseits können bestimmte Käferarten wie Laufkäfer (Carabidae) unter kälteren und trockeneren Bedingungen eine niedrige Luftfeuchtigkeit vertragen und sind in trockenen und halbtrockenen Regionen zu finden. Sie spielen als Räuber eine wichtige Rolle im Nahrungsnetz des Bodens und können auch bei der Schädlingsbekämpfung nützlich sein.
Darüber hinaus können bestimmte Spinnenarten wie die Wolfsspinnen (Lycosidae) niedrige Luftfeuchtigkeit tolerieren und sind in einer Vielzahl von Lebensräumen zu finden, darunter auch in trockenen Wüstenregionen.
Dies wären Spezies, die wir gegen Ende der Blüte verwenden können. Da sie damit sehr gut klarkommen als resistent sind. Es gibt allerdings auch Spezies, die zwar funktionieren, aber nicht ihre optimale Leistung unter diesen Bedingungen erfüllen können. Aber man kann trotzdem einsetzen oder sogar den optimal Leistenden vorziehen, wenn sie spezifische Beuteschemata haben, einfacher in der Handhabung sind oder weniger Einfluss auf die Blüte haben.
Phytoseiulus persimilis, ein Spinnmilbenräuber, der niedrige Luftfeuchtigkeit und kühle Temperaturen verträgt. Diese Art ist als wirksames biologisches Bekämpfungsmittel gegen Spinnmilben bekannt, die bei vielen Kulturpflanzen weit verbreitet sind und in trockenen Umgebungen gedeihen können.
Ein weiteres Beispiel ist Amblyseius californicus, eine Raubmilbe, die bei niedriger Luftfeuchtigkeit und niedrigen Temperaturen wirksam ist. Sie ernährt sich bekanntermaßen von verschiedenen Milben- und Thripsarten und hat sich in Gewächshäusern, Gärtnereien und im Freien bewährt.
Ein drittes Beispiel ist Neoseiulus cucumeris, eine Raubmilbenart, die sich von Thripsen und Spinnmilben ernährt. Sie verträgt sowohl niedrige Luftfeuchtigkeit als auch niedrige Temperaturen und wird häufig als biologisches Bekämpfungsmittel für Thripse in Gewächshäusern und im Freiland eingesetzt.
Es ist wichtig zu wissen, dass viele Arthropodenpopulationen lebensraumspezifisch sind, das heißt, dass bestimmte Arten in bestimmten Böden und Lebensräumen gedeihen. Es wäre von Vorteil, die lokalen Arthropodenpopulationen im Zielhabitat zu untersuchen, bevor man eine Art einführt, da sie möglicherweise nicht in der Lage ist, zu überleben oder sich an die neuen Bedingungen anzupassen.
Zudem kann zwischen Mikroarthropoden und Makroarthropoden unterschieden werden, diese unterscheiden sich hauptsächlich durch ihren Einfluss auf die gesamte Bodenstruktur. Makroarthropoden sind in der Lage, Bodenprofile umzustrukturieren oder große Mengen an Boden zu verlagern, während Mikroarthropoden in der Regel den Porenraum im Boden bewohnen (und nur wenig an dessen Veränderung mitwirken). Insbesondere Ameisen sind als Macroarthropoden beliebt, da sie mit ihren Gängen schon fast als Ökosystem ingenieure zählen. Sie sind outdoor von unermesslicher Wichtigkeit allerdings auch wieder im Indoor system zu Beginn zu aggressiv gegenüber den Sämlingen und in ihrer Art Blattläuse als Nutztiere zu halten.(Neher & Barbercheck, 2019) Spezies, welche für uns wirklich nutzbar sind, sind z.B. Spinnen wie die Wolfsspinne, welche z.B. auch bei Cranberries als Pathogenjäger eingesetzt wird. Hier sollte allerdings darauf geachtet werden entweder Spinnen zu wählen, welche in unserer Gegend vorkommen oder das System so geschlossen zu halten, dass ein Auskommen nicht möglich ist.
Befreiung des Bodens von Schwermetallen durch Mikroben
Mit einer Kombination aus verschiedenen Mikroben, können Verunreinigungen im Boden wie Schwermetalle gebunden und entfernt werden. Schwermetalle führen zum Durchfallen der Gesundheitstest im kommerziellen Anbau und führen bei Konsum zu starken Nervenschäden. Dies gilt es zu verhindern und deswegen ist ein kombinierter Ansatz von Nöten, um die Schwermetalle zu binden. Die wichtigsten Vertreter sind hier:
- Cadmium
- Chrom
- Quecksilber
- Nickel
- Blei
- Kupfer
- Zink
- Arsen
Cadmium ist hier in der geringsten und Zink in der höchsten Menge zugelassen, doch sollten sie alle präventiv vermieden oder kurativ für den Boden in Mikroben gebunden werden. Die meisten Schwermetalle sind auch für die hier erwähnten Spezies giftig, allerdings haben diese raffinierte Mechanismen zur Entgiftung durch Polymerisierung in Zellwänden oder Degradation durch Enzyme entwickelt. Dies macht sie auch unzugänglich für Pflanzen wie unserem besonders stark Schwermetall anreichenden Hanf. Die meisten können diese Abbauprodukte danach sogar für ihren Wuchs nutzen. So zerlegt Pleurotus ostreatus Erdöl unteranderem in Kalium. Die wichtigsten Organismen hierzu sind:
- Trichoderma ssp. = Blei, Cadmium und Arsen (Govarthanan et al. 2019; Zhang et al. 2018)
- Bacillus und Pseudomonas aeruginosa = Zink und Kupfer (Rajendran et al. 2003)
- Zooglea spp. und Citrobacter spp. = Kupfer, Nickel, Cadmium, Kobalt(Verma und Kuila 2019)
- Citrobacter spp. und Chlorella vulgaris = Cadmium, Blei, Uran, Kupfer, Nickel, Quecksilber, Uran (Rajendran et al. 2003)
- Aspergilus Niger = Cadmium, Thorium, Uran, Zink (Rajendran et al. 2003)
- Pleurotus ostreatus = Cadmium, Kupfer und Zink (Rajendran et al. 2003)
- Rhizopus arrhizus = Cadmium, Quecksilber, Blei(Rajendran et al. 2003)
- Stereum hirsutum = Cadmium, Kupfer, Kobalt, Nickel (Verma und Kuila 2019)
- Phormidium valderium = Cadmium; Blei (Verma und Kuila 2019)
- Ganoderma applantus = Kupfer, Blei, Quecksilber (Verma und Kuila 2019)
Die beste Übersicht, die ich zum generellen Thema Bioremediation durch weiße Rott-Pilze gefunden habe, ist: (Rajendran et al. 2003). Es sind auch viele weitere Einsatzwecke gelistet, wie z.B. die Umsetzung von Rohöl / Motoröl zu Pflanzennährstoffen und umweltverträglichen Mineralien.
Die wichtigsten Bioremediationsprozessen sind die Bioakkumulation, die Biolaugung, die Biosorption, die Biotransformation und die Biomineralisierung sowie die Wechselwirkungen zwischen Metall und Mikroben. Diese Prozesse ermöglichen es, die Schwermetalle ungefährlich zu machen (Verma und Kuila 2019). Dazu müssen allerdings bei manchen Spezies, welche es in ihren Fruchtkörpern einlagern, diese entfernt werden, da sonst im Falle des Absterbens des Pilzes die Metalle wieder zurück in den Boden gelangen.
Mikroorganismen sind nicht nur für die Metallauflösung, sondern auch für die Reduktion und Oxidation von Übergangsmetallen nützlich.
Abbildung 32: Mechanismen der Metalltoleranz bei Mikroben (Rajendran et al. 2003)
Pathogene Schadorganismen
Dieses Kapitel wird wahrscheinlich das sein, welches wir am kürzesten, im Vergleich zu seiner Größe, betrachten werden. Denn es gibt eigne Ausbildung zum Schädlingsbekämpfung Profi und das zusammen zufassen wäre wirklich utopisch.
Wir beschränken uns deshalb auf die Organismen mit den höchsten Schadenspotentialen und deren Verbreitung, Prävention und „Heilung“. Wir schauen uns jeweils 3 Beispiele für die 3 Gruppen Bakterien, Viren/Viroide und Pilze an. Dafür benötigen wir aber kurze Definitionen der wichtigsten Begriffe im Pflanzenschutz.
Bakterien
Xanthomonas campestris pv. cannabis
Die bakterielle Blattfleckenkrankheit von Hanf ist gekennzeichnet durch nekrotische Läsionen von ca. 1-2 mm Durchmesser mit einem gelben Halo von 2-3 mm Breite auf den Blättern. Es dringt durch Wunden in die Pflanze ein (Netsu et al. 2014). In manchen Kulturen wie Tomate induziert es zudem Schwarzrottung der Stämme, jedoch habe ich zu dieser Wirkung spezifisch in Cannabis noch keine Quelle gefunden.
Die Übertragung erfolgt über kontaminiertes Saatgut, Wasser und Geräte. Zu den Präventivmaßnahmen gehören die Verwendung von krankheitsfreiem Saatgut, die Sterilisierung von Geräten und die Vermeidung von Überkopfbewässerung.
Zwar dringen die Bakterien nicht in den Samen ein, können sich aber auf der Samenoberfläche ansiedeln und dort überdauern bis zur Keimung. Dort infizieren sie den Keimling am Ansatz und vernichten diesen.
Zu den kurativen Maßnahmen gehört der Einsatz von chemischen Bekämpfungsmethoden wie Kupferhydroxid, Streptomycin oder Oxytetracyclin. Dies ist allerdings nicht empfehlenswert im Living soil system, da jegliches Leben auch vernichtet wird. Bei Mutterpflanzen essenzieller Genetiken, die kein Backup haben, muss aber manchmal einfach zu solchen Mitteln gegriffen werden, um eine Rettung zu erzielen. Am besten isoliert ihr die Pflanze und sprüht nur unter Zuhilfenahme der adäquaten persönlichen Schutzausrüstung (PPE) und zugelassenen Menge (siehe Dünge/Pflanzenschutzverordnung)
Abbildung: 33 Symptome Xanthomonas campestris pv. cannabis (Netsu et al. 2014)
Pseudomonas cannabina
Dieses Bakterium verursacht die Blattfleckenkrankheit und Stammfäule bei Cannabispflanzen. Es infiziert die Blätter, die dadurch gelb und braun werden. Die Übertragung erfolgt über kontaminiertes Wasser und Geräte und ist Wirtspezifisch. (Bull et al. 2010)
Zu den Präventivmaßnahmen gehören die Verwendung von krankheitsfreiem Saatgut und die Sterilisierung von Geräten. Zu den kurativen Maßnahmen gehört der Einsatz von chemischen Bekämpfungsmethoden wie Kupferhydroxid, Streptomycin oder Oxytetracyclin.
Phytoplasma (PH)
Diese Gruppe von Bakterien verursacht die Hexenbesen-Krankheit bei Cannabispflanzen. Sie infiziert die Knospen der Pflanze und bewirkt, dass sie verkümmern und kleine, deformierte Blüten bilden. Die Übertragung erfolgt meist durch Insektenvektoren.
Zu den Präventivmaßnahmen gehören die Kontrolle der Vektorpopulationen, die Verwendung von krankheitsfreiem Saatgut und die Entfernung und Vernichtung von infiziertem Pflanzenmaterial.
Zu den kurativen Maßnahmen gehört der Einsatz chemischer Bekämpfungsmethoden wie Tetracyclin oder Streptomycin (Chaube et al. 2015).
Viren/Viroide
Latenter-Hopfen-Viroid (HLVd)
Dieses Virus gehört zur Gattung der Potyviren und verursacht latente Infektionen bei Cannabispflanzen. Viroide besitzen im Vergleich zu Viren keine schützende Proteinhülle und liegen als nackte RNA-Stränge vor.
Das heißt der Viroid kann im Virome der Pflanze vorliegen, aber keine aktiven Symptome zeigen, bis ein entsprechender Stress oder epigenetische Veränderungen die Infektion ausbrechen lassen. Zu den Symptomen gehören u. a. Verkümmerung, Missbildung oder Chlorose der Blätter, brüchige Stämme und Ertragsminderung bis zu 50%.
Die Chlorose und Ertragsminderung gehören zu den unspezifischen Symptomen, welche bei vielen Viren/Krankheiten auftreten. D.h. oft kann der Viroid nicht direkt durch Beobachtung identifiziert werden. Hierfür ist eine Rt-qPCR Analyse auf Viroid RNA Teilchen notwendig, um wirklich wissen zu können, dass es dieser spezifische Viroid ist.
Es wird durch kontaminierte Samen, Pollen, Vektoren (Insekten, die ihn aufnehmen und beim Anfressen der Pflanzen übertragen) und mechanisch (Scheren, Hände usw) übertragen.
Präventive Maßnahmen sind absolute Reinheit des Arbeitsgeräts, Verminderung der Pflanzenanfressenden Insektenpopulation und Quarantäne/Testung bei Aufnahme neuer Kultivare in die Anlage. (Warren et al. 2019; Flores et al. 2005; Chiginsky et al. 2021)
Heilung verspricht bisher rein die Meristemkultur in Kombination mit mehrfacher Testung an multiplen Pflanzenorganen und in verschiedenen Lebensabschnitten der Pflanze.
Durch molekulare Züchtung mithilfe von molekularen Markern, high throughput sequencing Technologien und großen Selektions/Diversitäts-populationen können resistente Kultivare gefunden und in die Elite Linien eingezüchtet werden. Dies benötigt tiefgreifendes Fachwissen und große Investionssummen, jedoch wäre dies umsetzbar und würde sein Invest hundertfach auszahlen. Meine Masterarbeit wird sich genau mit diesem Thema befassen und die ersten Forschungsarbeiten sind bereits in Progress.
Ein neues, aufstrebendes Startup in diesem Bereich ist die In Vitro / Biotechnology Firma AlpineBioLabs, welches sich gerade in Gründung befindet. Dies wird sämtliche Bereiche der Virus/Viroid Prävention, Behandlung und Forschung zu diesem Thema abdecken.
Nach Infektion eines Living soil Beets mit HLVd ist es leider notwendig die Erde zu entfernen. Es gibt sehr wenige Studien dazu allerdings kann gesagt werden, dass HLVd nur in lebenden Pflanzenteilen dauerhaft überleben kann. Jedoch arbeitet man oft mit Beipflanzen, welche dann ebenfalls infiziert werden können und damit dem Viroid Unterschlupf bieten. Genauere Studien werden hierfür benötigt, um zu bestimmen, wie lange das Viroid in toten Wurzeln überleben kann. Daher ist es essenziell es gar nicht erst zur Infektion kommen zu lassen, die Basis ist also ein ausgereiftes Präventionskonzept in Zusammenhang mit sauberem Ausgangsmaterial. Hierfür benötigt man entweder eine eigene Aufzucht mit monatlichen Tests und Quarantäneprogrammen oder einen Partner, der alle drei Monate frische, saubere Mutterpflanzen bereitstellt und eine umfangreiche, sichere Genbank mit Backups behält.
Auch hier wieder Werbung in eigener Sache, AlpineBioLabs wird sich diesen Herausforderungen stellen und versucht der vertrauenswürdige Partner zur Virus/Viroid Prävention/Behandlung im DACH/EU Raum zu werden.
Salat-Chlorose-Virus (LCV)
Dieses Virus gehört zur Gattung der Criniviren und der Familie der Closteroviridae
Es verursacht interveinale Chlorose, Sprödigkeit und gelegentlich Nekrose bei älteren Blättern bei Cannabispflanzen. Es wird durch den Vektor der Weißen Fliege übertragen. Zu den generellen Symptomen gehören Vergilbung und verkümmertes Wachstum der Pflanze.
Es gibt keine heilenden Maßnahmen für Virusinfektionen, daher sind vorbeugende Maßnahmen wie die Verwendung von krankheitsfreiem Saatgut und Geräten sowie die Kontrolle des Überträgers, der Weißen Fliege, von entscheidender Bedeutung für die Bekämpfung der Krankheit.
Wie bei fast allen Viren/Viroiden ist eine Meristemkultur mit integriertem Testprotokoll die Lösung. Hier kann Gewebe, welches nicht mit den Leitbahnen (Xylem/Phloem) verbunden ist, herausgeschnitten werden. Dieses Gewebe (Meristem) fungiert wie Stammzellen und aus ihnen können, jegliche Pflanzenorgane mithilfe von Organogenese differenziert werden.
Abbildung 34: "DurchSprossen übertragenes Cannabis-Salatchlorose-Virus (LCV).(a) Verkümmertes Wachstum einer Cannabispflanze, die aus LCV-infizierten Sprossen vermehrt wurde (links), im Vergleich zum Wachstum einer Cannabispflanze, die aus nicht infizierten Sprossen(rechts) (Hadad et al. 2019)
Cannabis cryptic virus (CanCV)
Das Cannabis Cryptic Virus (CanCV) ist ein Virus, das bei Cannabispflanzen die Symptome der "Hanfstreifenkrankheit" hervorruft. Das Virus, das derzeit das einzige bekannte Virus der Gattung Caulimovirus ist, welches Cannabis infiziert, wurde erstmals 2015 in Italien identifiziert.
Zu den Symptomen einer CanCV -Infektion gehören gelbe oder braune Streifen auf den Blättern, verkümmertes Wachstum und Ertragsminderung. Das Virus wird durch die Verwendung von infiziertem Pflanzmaterial sowie durch den Kontakt mit infizierten Pflanzenteilen übertragen.
Eine der wichtigsten Auswirkungen von CanCV auf den Gartenbau ist, dass es den Ertrag und die Qualität von Cannabispflanzen erheblich beeinträchtigen kann. Das Virus kann ein verkümmertes Wachstum verursachen, was zu kleineren Pflanzen mit weniger Blüten und geringeren THC- und CBD-Gehalten führen kann.
Eine weitere Auswirkung von CanCV ist, dass es schwierig sein kann, es zu bekämpfen. Bisher sind keine Studien zur mechanischen (horizontalen) Übertragung verfügbar. D.h. bisher geht man davon aus, dass es sich ausschließlich vertikal, also über Gameten (Pollen/Blüten) und somit Samen, übertragt (Righetti et al. 2018)
Gegenwärtig sind keine chemischen Behandlungsmethoden für CanCV bekannt, und die wirksamsten Bekämpfungsmaßnahmen bestehen in der Anwendung von Hygienemaßnahmen und der Verwendung von virusfreiem Pflanzmaterial.
Auch hier ist Meristemkultur die einzige kurative Lösung. (Ziegler et al. 2012)
Pilze
Botrytis cinerea (BC)
Dieser Pilz verursacht Grauschimmel an Cannabispflanzen. Er befällt die Blüten, Blätter und Stängel der Pflanze und verursacht Welkeerscheinungen und den Tod. Die Übertragung erfolgt durch Sporen, die durch Wind oder Wasser verbreitet werden. Zu den Präventivmaßnahmen gehören die Verwendung von krankheitsfreiem Saatgut, die Vermeidung von Überkopfbewässerung und die Entfernung und Vernichtung von infiziertem Pflanzenmaterial.
Dieser Pilz kann sowohl die lebende Pflanze als auch trocknende Blüten infizieren. Die meisten werden damit schon einmal Bekanntschaft gemacht haben. Das Wichtigste um eine Infektion zur Vermeiden sind neben der Übertragungsverhinderung, die Umweltbedingungen. Insbesondere freies Wasser, welches durch Kondensation auftritt, bietet den besten Nährboden für Botrytis. Es kann nicht nur durch Luftfeuchte allein überleben. D.h. entweder Pflanzensaft ist durch Schädigung des Gewebes (akuter Ca2+ Mangel + mechanische Einwirkung) ausgetreten oder eben Kondensat liegt vor.
Der komplette Verlust an Medizinischem Cannabis in Israel durch B. cinerea wird im Jahr auf 10% der Gesamtproduktion geschätzt (Jerushalmi et al. 2020)
Alternaria alternata
Alternaria alternata ist ein Pilzerreger, der eine Vielzahl von Pflanzenarten befallen kann, darunter auch Cannabis. Der Pilz verursacht eine Krankheit namens Alternaria-Blattfleckenkrankheit, die durch die Entwicklung von dunkelbraunen oder schwarzen Läsionen auf den Blättern, Stängeln und Blüten der Pflanze gekennzeichnet ist.
Der Pilz infiziert die Pflanze durch natürliche Öffnungen wie Spaltöffnungen oder Wunden, er kann aber auch über die Samen eindringen. Sobald der Pilz die Pflanze infiziert hat, beginnt er, Sporen zu produzieren, die durch Wind und Wasser verbreitet werden, so dass der Pilz neue Pflanzen infizieren kann.
Zu den Symptomen der Alternaria-Blattfleckenkrankheit gehört die Bildung dunkelbrauner oder schwarzer Läsionen auf den Blättern, Stängeln und Blüten der Pflanze. Diese Läsionen können in Größe und Form variieren und zu Blattvergilbung, Entlaubung und Absterben der Pflanze führen. Der Pilz kann auch die Knospen und Blüten infizieren und so den Ertrag und die Qualität der Ernte dramatisch verringern.
"Im August 2000 beispielsweise führte ein Ausbruch der durch A. alternata verursachten Blattfleckenkrankheit bei breitblättrigem Tabak (Nicotiana tabacum L.) zu einem Verlust von 75 % bzw. 89 % der gesamten Anbauflächen in Connecticut und Massachusetts.“ (LaMondia 2001)
Der Pilz kann auf Pflanzenresten überleben und im Boden über lange Zeiträume überleben. Es ist bekannt, dass der Pilz Pflanzen bei hoher relativer Luftfeuchtigkeit infizieren kann, so dass die Krankheit in feuchten Umgebungen stärker ausgeprägt ist.
Abbildung 35: (A) Alternaria alternata (Isolat 22A); (B) Botrytis cinerea (Isolat 63A); und (C) Kontrolle (Jerushalmi et al. 2020)
Fusarium oxysporum/solani
Fusarium oxysporum und Fusarium solani sind zwei verschiedene Arten des Pilzes Fusarium, die bekanntermaßen Pflanzenkrankheiten verursachen. Beide Arten können zwar eine Vielzahl von Pflanzenwirten infizieren und ähnliche Symptome hervorrufen z.B. Cannabis, doch gibt es einige Unterschiede bei den von ihnen verursachten Symptomen.
Fusarium oxysporum ist dafür bekannt, eine Krankheit namens Fusariumwelke zu verursachen, die durch Welken und Vergilben der Blätter und anschließendes Absterben der Pflanze gekennzeichnet ist. Dieser Erreger infiziert die Pflanze über das Wurzelsystem und kolonisiert den Stamm, was zum Welken und Absterben der Pflanze führt. Zu den Symptomen können auch Blattchlorose (Vergilbung) und eine Verkleinerung der Blätter, Blüten und Früchte gehören.
Fusarium solani hingegen ist dafür bekannt, eine Krankheit namens Fusarium-Kronenfäule zu verursachen, die durch Welken und Vergilben der Blätter und anschließendes Absterben der Pflanze gekennzeichnet ist. Dieser Erreger infiziert die Pflanze über das Wurzelsystem und kolonisiert den Stamm, was zum Welken und Absterben der Pflanze führt. Zu den Symptomen können auch Blattchlorose, Blattnekrose (Verbräunung) und eine Verringerung der Größe von Blättern, Blüten und Früchten gehören. Um diese Krankheitserreger zu bekämpfen, ist es wichtig, wirksame Strategien zur Krankheitsbekämpfung anzuwenden. Dazu gehören die regelmäßige Überwachung der Pflanzen auf Symptome einer Pilzinfektion, die Durchführung von Präventivmaßnahmen wie Fruchtfolge, Hygiene und die Verwendung von krankheitsfreiem Pflanzmaterial sowie der Einsatz von Fungiziden unter Anleitung eines Pflanzenpathologen oder eines anderen qualifizierten Fachmanns im äußersten Notfall. (Ali Merjan 2017)
Es ist wichtig, darauf hinzuweisen, dass weitere Forschungsarbeiten erforderlich sind, um neue und wirksame Strategien zur Bekämpfung dieser und anderer Pilzerreger, die medizinisches Cannabis befallen, zu ermitteln. Darüber hinaus könnte die Erforschung der genetischen und molekularen Merkmale dieser Krankheitserreger dazu beitragen, neue Wege zu ihrer Bekämpfung zu finden. (Jerushalmi et al. 2020)
Abbildung 36: (A) Nährsalzlösung Bilder intakter Pflanzen, einschließlich der Wurzeln von (C) einer mit Nährsalzlösung (Kontrolle) inokulierten Pflanze im Vergleich zu einer mit Fusarium oxysporum (Isolat 64B) inokulierten Pflanze (D). (Jerushalmi et al. 2020)
Dies waren jetzt nur Pathogene (bis auf botrytis) die auf lebende Pflanzen einwirken. Es gibt aber noch hunderte andere wie Asperagillus ssp. usw die Blüten kontaminieren können und auf die ebenfalls nach dem DAB getestet werden muss.
Endophyten
"Understanding Cultivar-Specificity and Soil Determinants of the Cannabis Microbiome" (Winston et al. 2014) und "Cannabis Microbiome and the Role of Endophytes in Modulating the Production of Secondary Metabolites: An Overview" (Taghinasab und Jabaji 2020) sind zwei aktuelle Studien, die die Beziehung zwischen dem endophytischen Mikrobiom von Cannabispflanzen und ihrem Wachstum sowie die Auswirkungen von Endophyten auf die Produktion von Sekundärmetaboliten in Cannabis untersuchen. Endophyten sind Mikroorganismen, die im Gewebe von Pflanzen leben und verschiedene positive Auswirkungen auf ihren Wirt haben können, wie z. B. eine erhöhte Resistenz gegen Krankheitserreger, eine verbesserte Nährstoffaufnahme und eine Modulation der Produktion von Sekundärmetaboliten.
Die erste Studie mit dem Titel "Understanding Cultivar-Specificity and Soil Determinants of the Cannabis Microbiome" konzentrierte sich auf zwei Hauptfaktoren, die das endophytische Mikrobiom von Cannabispflanzen beeinflussen könnten: Kulturspezifität und Bodendeterminanten. Die Forscher sammelten Proben von Cannabispflanzen, die in verschiedenen Böden und Sorten angebaut wurden, und verwendeten DNA-Sequenzierungstechniken, um die verschiedenen vorhandenen endophytischen Mikroorganismen zu identifizieren und zu quantifizieren.
Die Ergebnisse zeigten, dass das endophytische Mikrobiom von Cannabispflanzen tatsächlich sowohl von der Kulturspezifität als auch von Bodenfaktoren beeinflusst wurde. Verschiedene Cannabissorten wiesen unterschiedliche endophytische Mikrobiome auf, wobei einige Sorten eine größere Vielfalt an Mikroorganismen beherbergten als andere. Darüber hinaus waren die endophytischen Mikrobiome von Cannabispflanzen, die in verschiedenen Böden angebaut wurden, ebenfalls unterschiedlich, wobei einige Böden eine größere Vielfalt an Endophyten begünstigten als andere. Insbesondere Böden mit einem höheren Gehalt an organischen Stoffen förderten eine größere Vielfalt an endophytischen Mikroorganismen, insbesondere Proteobakterien, Actinobakterien und Bacteroidetes. Es hat sich gezeigt, dass diese Endophyten das Pflanzenwachstum fördern, indem sie pflanzenwachstumsfördernde Verbindungen wie Cytokinine und Indolessigsäure produzieren. Darüber hinaus wurde festgestellt, dass Böden mit neutralem pH-Wert (um 7) einen höheren Anteil an Endophyten aufweisen, die zu den Phyla Firmicutes und Acidobacteria gehören, die nachweislich die Nährstoffaufnahme der Pflanzen verbessern.
Die zweite Studie, "Cannabis Microbiome and the Role of Endophytes in Modulating the Production of Secondary Metabolites: Ein Überblick" konzentriert sich auf die Auswirkungen von Endophyten auf die Produktion von Sekundärmetaboliten in Cannabis. Die Studie ergab, dass endophytische Mikroorganismen die Produktion von Sekundärmetaboliten in Cannabis modulieren können, indem sie die Expression von Genen beeinflussen, die an der Biosynthese dieser Verbindungen beteiligt sind. Insbesondere wurde festgestellt, dass Endophyten, die zur Gattung Burkholderia gehören, positiv mit der Produktion von Sekundärmetaboliten in Cannabis wie Terpenoiden und Flavonoiden korrelieren. Diese Endophyten produzieren nachweislich Verbindungen wie Siderophore und Enzyme, die die Aufnahme von Eisen und anderen essenziellen Nährstoffen verbessern können, was wiederum zu einer Steigerung der Produktion von Sekundärmetaboliten führen könnte.
Eine andere Hypothese ist der Einfluss der Hormonproduktion von Endophyten. Das produzierte Gibberellin beeinflusst die Synthese von THC/CBD (terpenoidbasierten Stoffen) positiv indem sie 1-Aminocyclopropan-1-carbonsäurelevels regeln, was zu einer Erhöhung des Ethylenspiegels führt. (Mansouri et al. 2011)
Abbildung 37: "Die häufigsten Endophyten, die in verschiedenen Geweben von Cannabis sativa-Pflanzen aus unterschiedlichen geografischen Regionen vorkommen." (Robinson et al. 2016)
Ausblick
Dieser Stoff sollte nun für ein paar Wochen reichen, um sich zu beschäftigen, mich hat es mehrere Jahre des stetigen Lernens gekostet. Man muss nicht alles wissen und nicht alles verstehen, aber je besser man seine Werkzeuge als Grower versteht, desto besser werden auch die Ergebnisse.
Im nächsten Teil schauen wir uns dann an, wie man dieses theoretische Wissen in die Praxis umsetzt, um damit seinen eigenen Bodenmix zusammenstellen zu können. Es wird sich um eine tiefgehende Analyse der verschiedenen Substrate, Belüftungsmaterialien, Kompostformen, Fermente, Zusatzstoffe wie Biochar und viele weitere Amendments drehen. Zudem ist es gefüllt mit Referenzwerten zur Berechnung der späteren Bodeneigenschaften.
Den letzten Teil wird es dann im Laufe des Sommers nach den ersten Feldversuchen mit dem Bodenmix geben. Hier werden die laufenden Bedingungen simuliert und mit Bodentests abgeglichen. Einen Versuchsüberblick und Rechenbeispiele mit richtigen Feldwerten werden hier auch abgedeckt, um dann schlussendlich auf ein finales Rezept zu kommen, welches ihr dann selbst nachbauen könnt.
Literaturverzeichnis
A Chaos of Delight (2023): All about Collembola/springtails- Neelipleona - A Chaos of Delight. Online verfügbar unter https://www.chaosofdelight.org/all-about-collembola-neelipleona, zuletzt aktualisiert am 11.01.2023, zuletzt geprüft am 11.01.2023.
Abd-Elgawad, Mahfouz M. M.; Askary, Tarique Hassan; Coupland, James (2017): Biocontrol agents. Entomopathogenic and slug parasitic nematodes. Wallingford, Oxfordshire, UK, Boston, MA: CABI.
Agrios, George N. (2005): Plant pathology. 5th ed. Amsterdam: Elsevier Academic Press. Online verfügbar unter http://www.sciencedirect.com/science/book/9780120445653.
ALBRECHT, WILLIAM A. (1959): Soil Fertility and Animal Health. In: Soil Science 87 (5), S. 303. DOI: 10.1097/00010694-195905000-00014.
Ali Merjan (2017): The Fusarium Laboratory Manual. Online verfügbar unter https://www.researchgate.net/publication/321385629_The_Fusarium_Laboratory_Manual.
Andrews, Richard (2013): cationexchange. Online verfügbar unter http://www.zeoponix.com/cationexchange.htm, zuletzt aktualisiert am 28.11.2013, zuletzt geprüft am 09.01.2023.
Babu Ojha, Roshan; Devkota, Deepa (2014): Earthworms: 'Soil and Ecosystem Engineers' – a Review. In: WJAR 2 (6), S. 257–260. DOI: 10.12691/wjar-2-6-1.
Becker, Florian (2019): Herzbergs Zwei-Faktoren-Theorie der Motivation. In: Mitarbeiter wirksam motivieren: Springer, Berlin, Heidelberg, S. 57–65. Online verfügbar unter https://link.springer.com/chapter/10.1007/978-3-662-57838-4_8.
Bever, James D.; Schultz, Peggy A.; Pringle, Anne; Morton, Joseph B. (2001): Arbuscular Mycorrhizal Fungi: More Diverse than Meets the Eye, and the Ecological Tale of Why. In: BioScience 51 (11), S. 923. DOI: 10.1641/0006-3568(2001)051[0923:AMFMDT]2.0.CO;2.
Błaszkowski, J. (1994): Arbuscular fungi and mycorrhizae (Glomales) of the Hel Peninsula, Poland. In: Mycorrhiza 5 (1), S. 71–88. DOI: 10.1007/BF00204022.
Blume, Hans-Peter; Scheffer, Fritz; Schachtschabel, Paul (Hg.) (2010): Lehrbuch der Bodenkunde. 16., völlig neu bearb., aktualisierte und neu strukturierte Aufl. Heidelberg: Spektrum Akad. Verl. (Spektrum Lehrbuch).
Bonkowski, Michael (2004): Protozoa and plant growth: the microbial loop in soil revisited. In: New Phytologist 162 (3), S. 617–631. DOI: 10.1111/j.1469-8137.2004.01066.x.
Bull, Carolee T.; Manceau, Charles; Lydon, John; Kong, Hyesuk; Vinatzer, Boris A.; Fischer-Le Saux, Marion (2010): Pseudomonas cannabina pv. cannabina pv. nov., and Pseudomonas cannabina pv. alisalensis (Cintas Koike and Bull, 2000) comb. nov., are members of the emended species Pseudomonas cannabina (ex Sutic & Dowson 1959) Gardan, Shafik, Belouin, Brosch, Grimont & Grimont 1999. In: Systematic and Applied Microbiology 33 (3), S. 105–115. DOI: 10.1016/j.syapm.2010.02.001.
Burgel, Lisa; Hartung, Jens; Graeff-Hönninger, Simone (2020): Impact of Different Growing Substrates on Growth, Yield and Cannabinoid Content of Two Cannabis sativa L. Genotypes in a Pot Culture. In: Horticulturae 6 (4), S. 62. DOI: 10.3390/horticulturae6040062.
Campbell, Sean M.; Anderson, Steven L.; Brym, Zachary T.; Pearson, Brian J. (2021): Evaluation of substrate composition and exogenous hormone application on vegetative propagule rooting success of essential oil hemp (Cannabis sativa L.). In: PLoS ONE 16 (7), e0249160. DOI: 10.1371/journal.pone.0249160.
Carol, Rachel J.; Dolan, Liam (2002): Building a hair: tip growth in Arabidopsis thaliana root hairs. In: Philosophical transactions of the Royal Society of London. Series B, Biological sciences 357 (1422), S. 815–821. DOI: 10.1098/rstb.2002.1092.
Chaube, Savita; Kumar, Shailender; Dubey, Durgesh; Tiwari, Ajay Kumar; Upadhyaya, Parmatma Prasad; Rao, Govind Pratap (2015): Identification of a novel phytoplasma (16Sr XIV-A subgroup) associated with little leaf and witches’ broom of Cannabis sativa L. ssp. sativa and C. sativa L. ssp. indica in India. In: Phytoparasitica 43 (2), S. 275–279. DOI: 10.1007/s12600-014-0438-x.
Chet, I.; Ordentlich, A.; Shapira, R.; Oppenheim, A. (1990): Mechanisms of biocontrol of soil-borne plant pathogens by Rhizobacteria. In: Plant Soil 129 (1), S. 85–92. DOI: 10.1007/BF00011694.
Chiginsky, Judith; Langemeier, Kaitlyn; MacWilliams, Jacob; Albrecht, Tessa; Cranshaw, Whitney; Fulladolsa, Ana Cristina et al. (2021): First Insights Into the Virus and Viroid Communities in Hemp (Cannabis sativa). In: Front. Agron. 3, Artikel 778433, S. 96. DOI: 10.3389/fagro.2021.778433.
Cockson, Paul; Landis, Hunter; Smith, Turner; Hicks, Kristin; Whipker, Brian E. (2019a): Characterization of Nutrient Disorders of Cannabis sativa. In: Applied Sciences 9 (20), S. 4432. DOI: 10.3390/app9204432.
Cockson, Paul; Landis, Hunter; Smith, Turner; Hicks, Kristin; Whipker, Brian E. (2019b): Characterization of Nutrient Disorders of Cannabis sativa. In: Applied Sciences 9 (20), S. 4432. DOI: 10.3390/app9204432.
Couto, Daniel; Zipfel, Cyril (2016): Regulation of pattern recognition receptor signalling in plants. In: Nat Rev Immunol 16 (9), S. 537–552. DOI: 10.1038/nri.2016.77.
Deutscher Apotheker Verlag (2021): Deutsches Arzneibuch. Amtliche Ausgabe. Stuttgart, Eschborn, Berlin: Deutscher Apotheker Verlag; Avoxa - Mediengruppe Deutscher Apotheker; Akademie-Verl.
Deutscher Apotheker-Verlag Doktor Roland Schmiedel (2021): Deutsches Arzneibuch 2021 Digital. Amtliche Ausgabe (DAB 2021). 1. Auflage. Stuttgart: Deutscher Apotheker Verlag.
Devi, Rubee; Kaur, Tanvir; Kour, Divjot; Rana, Kusam Lata; Yadav, Ashok; Yadav, Ajar Nath (2020): Beneficial fungal communities from different habitats and their roles in plant growth promotion and soil health. In: MBJ 5 (1), S. 21–47. DOI: 10.21608/mb.2020.32802.1016.
Dmytryk, Agnieszka; Chojnacka, Katarzyna (2018): Algae As Fertilizers, Biostimulants, and Regulators of Plant Growth. In: Algae Biomass: Characteristics and Applications: Springer, Cham, S. 115–122. Online verfügbar unter https://link.springer.com/chapter/10.1007/978-3-319-74703-3_10.
Edwards, C. A.; Arancon, N. Q. (2004): Interactions among organic matter, earthworms, and microorganisms in promoting plant growth. In: Soil organic matter in sustainable agriculture, S. 327–376.
Esteban, Raquel; Ariz, Idoia; Cruz, Cristina; Moran, Jose Fernando (2016): Review: Mechanisms of ammonium toxicity and the quest for tolerance. In: Plant science : an international journal of experimental plant biology 248, S. 92–101. DOI: 10.1016/j.plantsci.2016.04.008.
Etesami, Hassan; Alikhani, Hossein Ali; Hosseini, Hossein Mirseyed (2015): Indole-3-acetic acid (IAA) production trait, a useful screening to select endophytic and rhizosphere competent bacteria for rice growth promoting agents. In: MethodsX 2, S. 72–78. DOI: 10.1016/j.mex.2015.02.008.
Flores, Ricardo; Hernández, Carmen; Martínez de Alba, A. Emilio; Daròs, José-Antonio; Di Serio, Francesco (2005): Viroids and viroid-host interactions. In: Annual review of phytopathology 43, S. 117–139. DOI: 10.1146/annurev.phyto.43.040204.140243.
Geelen, P. A. M.; Voogt, J. O.; van Weel, P. A. (2019): Plant empowerment. The basic principles : how an integrated approach based on physics and plant physiology leads to balanced growing method for protected crops resulting in healthy resilient plants, high yield and quality, low energy costs and economic greenhouse concepts. [Vlaardingen]: Letsgrow.com.
Goswami, Dweipayan; Thakker, Janki N.; Dhandhukia, Pinakin C. (2016): Portraying mechanics of plant growth promoting rhizobacteria (PGPR): A review. In: Cogent Food & Agriculture 2 (1). DOI: 10.1080/23311932.2015.1127500.
Govarthanan, M.; Mythili, R.; Kamala-Kannan, S.; Selvankumar, T.; Srinivasan, P.; Kim, H. (2019): In-vitro bio-mineralization of arsenic and lead from aqueous solution and soil by wood rot fungus, Trichoderma sp. In: Ecotoxicology and Environmental Safety 174, S. 699–705. DOI: 10.1016/j.ecoenv.2019.03.034.
Hadad, Lior; Luria, Neta; Smith, Elisheva; Sela, Noa; Lachman, Oded; Dombrovsky, Aviv (2019): Lettuce Chlorosis Virus Disease: A New Threat to Cannabis Production. In: Viruses 11 (9), S. 802. DOI: 10.3390/v11090802.
Hammer, P. E.; Hill, D. S.; Lam, S. T.; van Pée, K. H.; Ligon, J. M. (1997): Four genes from Pseudomonas fluorescens that encode the biosynthesis of pyrrolnitrin. In: Applied and Environmental Microbiology 63 (6), S. 2147–2154. DOI: 10.1128/aem.63.6.2147-2154.1997.
Hartemink, Alfred E.; Barrow, N. J. (2023): Soil pH - nutrient relationships: the diagram. In: Plant Soil, S. 1–7. DOI: 10.1007/s11104-022-05861-z.
Helliwell, J. R.; Miller, A. J.; Whalley, W. R.; Mooney, S. J.; Sturrock, C. J. (2014): Quantifying the impact of microbes on soil structural development and behaviour in wet soils. In: Soil Biology and Biochemistry 74, S. 138–147. DOI: 10.1016/j.soilbio.2014.03.009.
Hossain, Md. Motaher; Sultana, Farjana; Islam, Shaikhul (2017): Plant Growth-Promoting Fungi (PGPF): Phytostimulation and Induced Systemic Resistance. In: Plant-Microbe Interactions in Agro-Ecological Perspectives: Springer, Singapore, S. 135–191. Online verfügbar unter https://link.springer.com/chapter/10.1007/978-981-10-6593-4_6.
International Peatland Society (2019): What is peat? - International Peatland Society. Online verfügbar unter https://peatlands.org/peat/peat/, zuletzt aktualisiert am 02.07.2019, zuletzt geprüft am 16.04.2023.
JAKOBSEN, I.; ABBOTT, L. K.; ROBSON, A. D. (1992): External hyphae of vesicular-arbuscular mycorrhizal fungi associated with Trifolium subterraneum L. 1. Spread of hyphae and phosphorus inflow into roots. In: New Phytologist 120 (3), S. 371–380. DOI: 10.1111/j.1469-8137.1992.tb01077.x.
Jerushalmi, Shachar; Maymon, Marcel; Dombrovsky, Aviv; Freeman, Stanley (2020): Fungal Pathogens Affecting the Production and Quality of Medical Cannabis in Israel. In: Plants 9 (7), S. 882. DOI: 10.3390/plants9070882.
Kim, J.; Jiang, X. (2010): The growth potential of Escherichia coli O157:H7, Salmonella spp. and Listeria monocytogenes in dairy manure-based compost in a greenhouse setting under different seasons. In: Journal of Applied Microbiology 109 (6), S. 2095–2104. DOI: 10.1111/j.1365-2672.2010.04841.x.
Küstermann, B., Kainz, M. & Hülsbergen, K.‑J. (2008). Modeling carbon cycles and estimation of greenhouse gas emissions from organic and conventional farming systems. Renewable Agriculture and Food Systems, 23(1), 38–52. https://doi.org/10.1017/S1742170507002062
LaMondia, J. A. (2001): Outbreak of Brown Spot of Tobacco Caused by Alternaria alternata in Connecticut and Massachusetts. In: Plant Disease 85 (2), S. 230. DOI: 10.1094/PDIS.2001.85.2.230B.
Landi, S. (1997): Mineral nutrition of Cannabis sativa L. In: Journal of Plant Nutrition 20 (2-3), S. 311–326. DOI: 10.1080/01904169709365252.
Lavelle, P. (1988): Earthworm activities and the soil system. In: Biol Fert Soils 6 (3), S. 237–251. DOI: 10.1007/BF00260820.
Li, Wei; Xiang, Fen; Zhong, Micai; Zhou, Lingyun; Liu, Hongyan; Li, Saijun; Wang, Xuewen (2017): Transcriptome and metabolite analysis identifies nitrogen utilization genes in tea plant (Camellia sinensis). In: Sci Rep 7 (1), S. 1693. DOI: 10.1038/s41598-017-01949-0.
Lin, Y. S.; Heuer, V. B.; Ferdelman, T. G.; Hinrichs, K.-U. (2010): Microbial conversion of inorganic carbon to dimethyl sulfide in anoxic lake sediment (Plußsee, Germany). In: Biogeosciences 7 (8), S. 2433–2444. DOI: 10.5194/bg-7-2433-2010.
Llewellyn, David; Golem, Scott; Jones, A. Maxwell P.; Zheng, Youbin (2023): Foliar Symptomology, Nutrient Content, Yield, and Secondary Metabolite Variability of Cannabis Grown Hydroponically with Different Single-Element Nutrient Deficiencies. In: Plants 12 (3), S. 422. DOI: 10.3390/plants12030422.
LOACH, K. (1985): Rooting of cuttings in relation to the propagation medium. In: (35), S. 472–485. Online verfügbar unter https://pascal-francis.inist.fr/vibad/index.php?action=getRecordDetail&idt=8244846.
Local Land Services (NSW Government) (2020): Cation Exchange Capacity. Fact Sheet 4.
Logan Labs (2023): Logan Labs Soil Testing Services | Lakeview Ohio, zuletzt aktualisiert am 01.04.2023, zuletzt geprüft am 01.04.2023.
Lowenfels, Jeff; Lewis, Wayne (Hg.) (2016): Teaming with microbes. The organic gardener's guide to the soil food web. Revised edition. Portland, Or.: Timber Press.
Maathuis, Frans J. M.; Diatloff, Eugene (2013): Roles and functions of plant mineral nutrients. In: Methods in molecular biology (Clifton, N.J.) 953, S. 1–21. DOI: 10.1007/978-1-62703-152-3_1.
Mansouri, Hakimeh; Asrar, Zahra; Amarowicz, Ryszard (2011): The response of terpenoids to exogenous gibberellic acid in Cannabis sativa L. at vegetative stage. In: Acta Physiol Plant 33 (4), S. 1085–1091. DOI: 10.1007/s11738-010-0636-1.
Naitam, Mayur G.; Kaushik, Rajeev (2021): Archaea: An Agro-Ecological Perspective. In: Current microbiology 78 (7), S. 2510–2521. DOI: 10.1007/s00284-021-02537-2.
Natural Resources Conservation Service (2023): Soil Classification | Natural Resources Conservation Service. Online verfügbar unter https://www.nrcs.usda.gov/resources/guides-and-instructions/soil-classification, zuletzt aktualisiert am 11.01.2023, zuletzt geprüft am 11.01.2023.
Netsu, Osamu; Kijima, Toshio; Takikawa, Yuichi (2014): Bacterial leaf spot of hemp caused by Xanthomonas campestris pv. cannabis in Japan. In: J Gen Plant Pathol 80 (2), S. 164–168. DOI: 10.1007/s10327-013-0497-8.
Niu, Dong-Dong; Wang, Chun-Juan; Guo, Ya-Hui; Jiang, Chun-Hao; Zhang, Wen-Zhi; Wang, Yun-peng; Guo, Jian-Hua (2012): The plant growth-promoting rhizobacterium Bacillus cereus AR156 induces resistance in tomato with induction and priming of defence response. In: Biocontrol Science and Technology 22 (9), S. 991–1004. DOI: 10.1080/09583157.2012.706595.
Oswald, Iain W. H.; Ojeda, Marcos A.; Pobanz, Ryan J.; Koby, Kevin A.; Buchanan, Anthony J.; Del Rosso, Josh et al. (2021): Identification of a New Family of Prenylated Volatile Sulfur Compounds in Cannabis Revealed by Comprehensive Two-Dimensional Gas Chromatography. In: ACS Omega 6 (47), S. 31667–31676. DOI: 10.1021/acsomega.1c04196.
Palm, Juliane; van Schaik, N. Loes M.B.; Schröder, Boris (2013): Modelling distribution patterns of anecic, epigeic and endogeic earthworms at catchment-scale in agro-ecosystems. In: Pedobiologia 56 (1), S. 23–31. DOI: 10.1016/j.pedobi.2012.08.007.
Pandey, Nalini (2018): Role of Plant Nutrients in Plant Growth and Physiology. In: Plant Nutrients and Abiotic Stress Tolerance: Springer, Singapore, S. 51–93. Online verfügbar unter https://link.springer.com/chapter/10.1007/978-981-10-9044-8_2.
Park, K-H; Lee, C-Y; Son, H-J (2009): Mechanism of insoluble phosphate solubilization by Pseudomonas fluorescens RAF15 isolated from ginseng rhizosphere and its plant growth-promoting activities. In: Letters in applied microbiology 49 (2), S. 222–228. DOI: 10.1111/j.1472-765X.2009.02642.x.
Peterson, J. C. (1982): Effects of pH [hydrogen-ion concentration] upon nutrient availability in a commercial soilless root medium utilized for floral crop production. Online verfügbar unter https://agris.fao.org/agris-search/search.do?recordid=us19830871517.
Płociniczak, T.; Kukla, M.; Wątroba, R.; Piotrowska-Seget, Z. (2013): The effect of soil bioaugmentation with strains of Pseudomonas on Cd, Zn and Cu uptake by Sinapis alba L. In: Chemosphere 91 (9), S. 1332–1337. DOI: 10.1016/j.chemosphere.2013.03.008.
Rajendran, P.; Muthukrishnan, J.; Gunasekaran, P. (2003): Microbes in heavy metal remediation. In: 0975-1009. Online verfügbar unter https://nopr.niscpr.res.in/handle/123456789/17153.
Rasool, Saiema; Ahmad, Altaf; Siddiqi, T. O.; Ahmad, Parvaiz (2013): Changes in growth, lipid peroxidation and some key antioxidant enzymes in chickpea genotypes under salt stress. In: Acta Physiol Plant 35 (4), S. 1039–1050. DOI: 10.1007/s11738-012-1142-4.
Remy, W.; Taylor, T. N.; Hass, H.; Kerp, H. (1994): Four hundred-million-year-old vesicular arbuscular mycorrhizae. In: Proceedings of the National Academy of Sciences of the United States of America 91 (25), S. 11841–11843. DOI: 10.1073/pnas.91.25.11841.
Righetti, Laura; Paris, Roberta; Ratti, Claudio; Calassanzio, Matteo; Onofri, Chiara; Calzolari, Davide et al. (2018): Not the one, but the only one: about Cannabis cryptic virus in plants showing ‘hemp streak’ disease symptoms. In: Eur J Plant Pathol 150 (3), S. 575–588. DOI: 10.1007/s10658-017-1301-y.
Rillig, Matthias C.; Mummey, Daniel L. (2006): Mycorrhizas and soil structure. In: The New phytologist 171 (1), S. 41–53. DOI: 10.1111/j.1469-8137.2006.01750.x.
Robinson, Rebekah J.; Fraaije, Bart A.; Clark, Ian M.; Jackson, Robert W.; Hirsch, Penny R.; Mauchline, Tim H. (2016): Wheat seed embryo excision enables the creation of axenic seedlings and Koch's postulates testing of putative bacterial endophytes. In: Sci Rep 6 (1), S. 25581. DOI: 10.1038/srep25581.
Sasse, Joelle; Martinoia, Enrico; Northen, Trent (2018): Feed Your Friends: Do Plant Exudates Shape the Root Microbiome? In: Trends in Plant Science 23 (1), S. 25–41. DOI: 10.1016/j.tplants.2017.09.003.
Schrader, Stefan; Zhang, Haiquan (1997): Earthworm casting: Stabilization or destabilization of soil structure? In: Soil Biology and Biochemistry 29 (3-4), S. 469–475. DOI: 10.1016/S0038-0717(96)00103-4.
St. Croix Sensory Inc. (2018): Parameters of Odor. In: St. Croix Sensory, Inc., 03.01.2018. Online verfügbar unter https://www.fivesenses.com/Documents/Library/StCroixSensory_Odor_Parameters_Copyright2018.pdf, zuletzt geprüft am 19.09.2022.
Stevenson, Frank J. (1994): Humus chemistry. Genesis, composition, reactions. 2. ed. New York: Wiley.
Taghinasab, Meysam; Jabaji, Suha (2020): Cannabis Microbiome and the Role of Endophytes in Modulating the Production of Secondary Metabolites: An Overview. In: Microorganisms 8 (3), S. 355. DOI: 10.3390/microorganisms8030355.
Tegeder, Mechthild; Rentsch, Doris (2010): Uptake and partitioning of amino acids and peptides. In: Molecular plant 3 (6), S. 997–1011. DOI: 10.1093/mp/ssq047.
Turunen, M.; Hyväluoma, J.; Heikkinen, J.; Keskinen, R.; Kaseva, J.; Koestel, J.; Rasa, K. (2019): Quantifying Physical Properties of Three Sphagnum ‐Based Growing Media as Affected by Drying–Wetting Cycles. In: Vadose zone j. 18 (1), S. 190033. DOI: 10.2136/vzj2019.04.0033.
Verma, Samakshi; Kuila, Arindam (2019): Bioremediation of heavy metals by microbial process. In: Environmental Technology & Innovation 14, S. 100369. DOI: 10.1016/j.eti.2019.100369.
Wang, H.; Inukai, Y.; Yamauchi, A. (2006): Root Development and Nutrient Uptake. In: Critical Reviews in Plant Sciences 25 (3), S. 279–301. DOI: 10.1080/07352680600709917.
Warren, J. G.; Mercado, J.; Grace, D. (2019): Occurrence of Hop Latent Viroid Causing Disease in Cannabis sativa in California. In: Plant Disease 103 (10), S. 2699. DOI: 10.1094/PDIS-03-19-0530-PDN.
Weigend, Maximilian; Mustafa, Adeel; Ensikat, Hans-Jürgen (2018): Calcium phosphate in plant trichomes: the overlooked biomineral. In: Planta 247 (1), S. 277–285. DOI: 10.1007/s00425-017-2826-1.
Winston, Max E.; Hampton-Marcell, Jarrad; Zarraonaindia, Iratxe; Owens, Sarah M.; Moreau, Corrie S.; Gilbert, Jack A. et al. (2014): Understanding cultivar-specificity and soil determinants of the cannabis microbiome. In: PLOS ONE 9 (6), e99641. DOI: 10.1371/journal.pone.0099641.
Zhang, Xu; Li, Xinxin; Yang, Huanhuan; Cui, Zhaojie (2018): Biochemical mechanism of phytoremediation process of lead and cadmium pollution with Mucor circinelloides and Trichoderma asperellum. In: Ecotoxicology and Environmental Safety 157, S. 21–28. DOI: 10.1016/j.ecoenv.2018.03.047.
Ziegler, Angelika; Matoušek, Jaroslav; Steger, Gerhard; Schubert, Jörg (2012): Complete sequence of a cryptic virus from hemp (Cannabis sativa). In: Arch Virol 157 (2), S. 383–385. DOI: 10.1007/s00705-011-1168-8.